题目内容
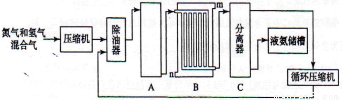
以铬酸钾为原料,电化学法制备重铬酸钾的实验装置示意图如下:
下列说法不正确的是

A.在阴极式,发生的电极反应为:2H2O+2e- 2OH―+H2↑
2OH―+H2↑
B.在阳极室,通电后溶液逐渐由黄色变为橙色,是因为阳极区H+浓度增大,使平衡2 +2H+
+2H+
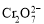 +H2O向右移动
+H2O向右移动
C.该制备过程总反应的化学方程式为:4K2CrO4+4H2O 2K2Cr2O7+4KOH+2H2↑+2O2↑
2K2Cr2O7+4KOH+2H2↑+2O2↑
D.测定阳极液中K和Cr的含量,若K与Cr的物质的量之比为d,则此时铬酸钾的转化率为α=
D
【解析】本题是电解法在制备物质中的具体应用。分析该制备时,重点要把握其中的K2CrO4在转变为K2Cr2O7的过程中没有发生化合价的变化,所以要抓住是由于溶液的pH变化实现目标物的合成,制备的过程是通过电解的方法改变溶液的pH来实现。阴极的反应是 2H2O+2e-=2OH-+H2,阳极为2H2O-4e-=O2+4H+,电解过程中阳极区的c(H+)增大,促进平衡2CrO42-+2H+= Cr2O72-+H2O向右移动,总反应为4 K2CrO4+4H2O=2 K2Cr2O7+4KOH+2H2↑+O2↑;若设加入反应容器内的K2CrO4有1mol,反应中有x mol K2CrO4转化为K2Cr2O7,则阳极区剩余的K2CrO4为(1-x) mol,对应的n(K)=2(1-x) mol,n(Cr)= (1-x) mol,生成的K2Cr2O7为x/2 mol,,对应的n(K)= x mol,n(Cr)= x mol,由n(K)/ n(Cr)=d可得,x=2-d,转化率为(2-d)/1。
【考点定位】本题通过制备重铬酸钾考查电化学知识。

 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案[15分]甲烷自热重整是先进的制氢方法,包含甲烷氧化和蒸汽重整。向反应系统同时通入甲烷、氧气和水蒸气,发生的主要化学反应有:
反应过程 | 化学方程式 | 焓变△H (kJ/mol) | 活化能Ea (kJ/mol) |
甲烷氧化 | CH4(g)+2O2(g) | -802.6 | 125.6 |
CH4(g)+O2(g) | -322.0 | 172.5 | |
蒸汽重整 | CH4(g)+H2O(g) | 206.2 | 240.1 |
CH4(g)+2H2O(g) | 165.0 | 243.9 |
回答下列问题:
(1)反应CO(g)+H2O(g) CO2(g)+H2(g)的△H= kJ/mol。
CO2(g)+H2(g)的△H= kJ/mol。
(2)在初始阶段,甲烷蒸汽重整的反应速率 甲烷氧化的反应速率(填大于、小于或等于)。
(3)对于气相反应,用某组分(B)的平衡压强(PB)代替物质的量浓度(cB)也可以平衡常数(记作KP),则反应CH4(g)+H2O(g) CO(g)+3H2(g)的KP= ;
CO(g)+3H2(g)的KP= ;
随着温度的升高,该平衡常数 (填“增大”、“减小”或“不变”)。
(4)从能量阶段分析,甲烷自热重整方法的先进之处在于 。
(5)在某一给定进料比的情况下,温度、压强对H2和CO物质的量分数的影响如下图:
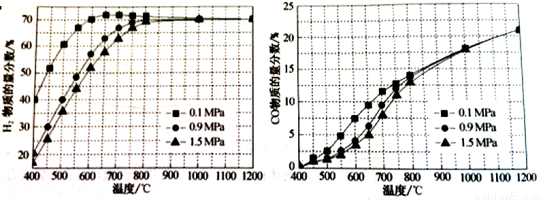
①若要达到H2物质的量分数>65%、CO的物质的量分数<10%,以下条件中最合适的是 。
A.600℃,0.9MpaB.700℃,0.9MPaC.800℃,1.5MpaD.1000℃,1.5MPa
②画出600℃,0.1Mpa条件下,系统中H2物质的量分数随反应时间(从常温进料开始即时)
的变化趋势示意图:
(6)如果进料中氧气量过大,最终导致H2物质的量分数降低,原因是 。