题目内容
(4分)相同条件下,H2、N2两种气体按体积比为2∶1的比例混合,所得混合气体中N2质量为1.4g,问:
(1)该混合气体的总质量为多少?
(2)该混合气体在标准状况下的体积为多少?
(1)该混合气体的总质量为多少?
(2)该混合气体在标准状况下的体积为多少?
1.6g, 3.36L
(1)n(N2)= =
= =0.05mol
=0.05mol
∵相同条件下,气体的体积比等于物质的量之比
∴n(H2)="2" n(N2)=2×0.05mol= 0.1mol
0.1mol
∴m(混)=1.4g+0.1mol×2g·mol-1=1.6g(2分)
(2)V(混)=n(混)×Vm=(0.05mol+0.1mol)×22.4L·mol-1=3.36L(2分)
 =
= =0.05mol
=0.05mol∵相同条件下,气体的体积比等于物质的量之比
∴n(H2)="2" n(N2)=2×0.05mol=
 0.1mol
0.1mol∴m(混)=1.4g+0.1mol×2g·mol-1=1.6g(2分)
(2)V(混)=n(混)×Vm=(0.05mol+0.1mol)×22.4L·mol-1=3.36L(2分)

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
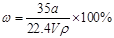 ②
②