题目内容
下列离子方程式中,正确的是( )
| A.稀硫酸滴在铁片上:2Fe+6H+=Fe3++3H2↑ |
| B.氢氧化镁与稀盐酸反应:OH?+H+=H2O |
| C.碳酸氢钠溶液与稀盐酸混合:HCO3?+H+=H2O+CO2↑ |
| D.硫酸铜溶液与氢氧化钡溶液混合:Cu2++2OH?=Cu(OH)2↓ |
C
解析试题分析:A. Fe+2H+=Fe2++H2↑;B,氢氧化镁难溶于水,不能拆成离子形式;D.硫酸铜溶液与氢氧化钡溶液混合:SO42?+Cu2++ Ba2++2OH?=Cu(OH)2↓+ BaSO4↓。只有C正确。
考点:离子方程式的正误判断。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
常温下,下列各组离子在指定溶液中一定能大量共存的是:
| A.能使淀粉-KI试纸显蓝色的溶液中:K+ SO42- S2- SO32- |
| B.含有0.1mol·L-1 Fe2+的溶液:Na+Cl- ClO- SO42- |
| C.c(H+)/c(OH-)=1012的溶液中:Al3+ NH4+ NO3- K+ |
| D.含有0.1mol·L-1 HCO3-的溶液:Na+ Fe3+ NO3- C6H5O- |
在下列各溶液中,离子一定能大量共存的是( )
| A.强碱性溶液中:K+、Al3+、Cl-、SO42- |
B.含有0.1 mol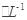 Fe3+的溶液中:K+、Mg2+、I-、NO3- Fe3+的溶液中:K+、Mg2+、I-、NO3- |
C.含有0.1mol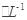 Ca2+溶液在中:Na+、K+、CO32-、Cl- Ca2+溶液在中:Na+、K+、CO32-、Cl- |
| D.室温下,pH=l的溶液中:Na+、Fe3+、NO3-、SO42- |
某溶液与过量的NH4HCO3溶液混合加热,既有气体生成,又有沉淀生成,则此溶液可能大量共存的离子组是 ( )
| A.K+ Cl- SO42- Ba2+ H+ | B.Mg2+ NO3- SO42- OH-Na+ |
| C.Mg2+ Na+ Cl- H+ NO3- | D.Na+ Ba2+ NO3- OH- Cl- |
某溶液中存在较多的H+、SO42-、C1-,该溶液中还可能大量存在的离子是
| A.OH- | B.Ba2+ | C.NH4+ | D.Ag+ |
下列离子方程式与所述事实相符且正确的是( )
| A.Ca(OH)2悬浊液中滴加足量稀硝酸:H++OH-=H2O |
| B.Ca(HCO3)2溶液中加入少量NaOH溶液:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+H2O |
| C.硫酸氢钠溶液中加入Ba(OH)2溶液至SO42-恰好完全沉淀:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O |
| D.向含有0.4 mol FeBr2的溶液中通入0.3 mol Cl2充分反应:4Fe2++2Br-+3Cl2=4Fe3++6Cl-+Br2 |
(原创)在遇铝粉能产生大量气体的溶液中,可能大量共存的是
| A.Fe2+、Cl-、NO3-、CH3COO- | B.Na+、Ca2+、Cl-、CO32- |
| C.Na+、SO42-、NH4+、HCO3- | D.Na+、K+、NO3-、CO32- |
下列各组离子一定能在无色溶液中大量共存的是
| A.Na+、CO32-、NO3-、AlO2- | B.K+、H+、CrO42-、SO32- |
| C.Al3+、Ba2+、HCO3-、Cl- | D.Fe3+、Mg2+、SCN-、Cl- |
物质之间相互反应时,加入的量不同往往反应不尽相同,在给定条件下反应,下列叙述 正确的是( )
A.NaHCO3与石灰水反应,当n(NaHCO3):n[Ca(OH)2]=1︰1时,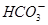 完全转化为CaCO3 完全转化为CaCO3 |
| B.CO2通入石灰水中,当n(CO2)︰n[Ca(OH)2]=1︰1时,能得到澄清溶液 |
C.AlCl3溶液与烧碱溶液反应,当n(OH-)︰n(Al3+)=1︰1时,铝元素以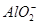 形式存在 形式存在 |
| D.Fe与稀硝酸反应,当n(Fe)︰n(HNO3)=1︰1时,溶液中铁元素只以Fe3+形式存在 |