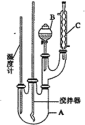题目内容
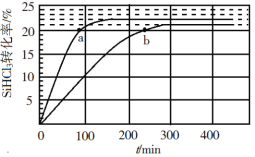
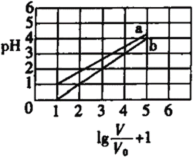
【题目】次磷酸(H3PO2,一元弱酸)和氟硼酸(HBF4)均可用于植物杀菌。常温时,有1 mol L-1的H3PO2溶液和1 mol˙L-1的HBF4溶液,两者起始时的体积均为V0,分别向两溶液中加水,稀释后溶液的体积均为V,两溶液的pH变化曲线如图所示.下列说法错误的是:
A.常温下,该HBF4溶液满足pH=![]()
B.常温下,H3PO2的电离平衡常数约为1.1![]() 10-2
10-2
C.常温下,NaBF4溶液的pH=7
D.NaH2PO2溶液中:c(OH-)-c(H+) =c(H3PO2)
【答案】A
【解析】
当![]() +1=1时,V=V0,即起始时1mol/L的曲线b溶液的pH=0,说明曲线b对应酸为强酸,H3PO2为一元弱酸,则曲线b为氟硼酸(HBF4)加水稀释的曲线,曲线a为H3PO2溶液的稀释曲线,据此分析。
+1=1时,V=V0,即起始时1mol/L的曲线b溶液的pH=0,说明曲线b对应酸为强酸,H3PO2为一元弱酸,则曲线b为氟硼酸(HBF4)加水稀释的曲线,曲线a为H3PO2溶液的稀释曲线,据此分析。
A.根据图示曲线b可知,![]() +1=1,则
+1=1,则![]() =pH=0,
=pH=0,![]() +1=5时,
+1=5时,![]() =pH=4,所以在0pH4时,HBF4溶液满足pH=
=pH=4,所以在0pH4时,HBF4溶液满足pH=![]() ,故A错误;
,故A错误;
B.a曲线表示的是次磷酸的稀释曲线,由曲线上的点的坐标可知,1mol/L的次磷酸溶液的pH=1,即c(H+)=0.1mol/L;次磷酸电离方程式为:H3PO2H+ +H2PO2-,所以1mol/L的次磷酸溶液中c(H3PO2)=0.9mol/L,c(H2PO2-)=0.1mol/L,那么次磷酸的电离平衡常数即为:
Ka![]() ,故B正确;
,故B正确;
C.根据图像可知,b表示的酸每稀释十倍,pH值增加1,所以b为强酸的稀释曲线,又因为H3PO2为一元弱酸,所以b对应的酸只能是氟硼酸(HBF4),即氟硼酸为强酸;那么NaBF4即为强酸强碱盐,故溶液为中性,常温下pH=7,C项正确;
D.NaH2PO2溶液中:符合质子守恒,c(OH-)=c(H3PO2)+c(H+),则c(OH-)-c(H+) =c(H3PO2),故D正确;
答案选A。

 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案【题目】某小组同学探究物质的溶解度大小与沉淀转化方向之间的关系。已知:
物质 | BaSO4 | BaCO3 | AgI | AgCl | |
溶解度/g(20℃) | 2.4×10-4 | 1.4×10-3 | 3.0×10-7 | 1.5×10-4 |
(1)探究BaCO3和BaSO4之间的转化
实验操作:
试剂A | 试剂B | 试剂C | 加入盐酸后的现象 | |
实验Ⅰ | BaCl2 | Na2CO3 | Na2SO4 | …… |
实验Ⅱ | Na2SO4 | Na2CO3 | 有少量气泡产生,沉淀部分溶解 |
① 实验Ⅰ说明BaCO3全部转化为BaSO4,依据的现象是加入盐酸后,______。
② 实验Ⅱ中加入稀盐酸后发生反应的离子方程式是______。
③ 实验Ⅱ说明沉淀发生了部分转化,结合BaSO4的沉淀溶解平衡解释原因:______。
(2)探究AgCl和AgI之间的转化
实验Ⅲ:
实验Ⅳ:在试管中进行溶液间反应时,同学们无法观察到AgI转化为AgCl,于是又设计了如下实验(电压表读数:a>c>b>0)。
装置 | 步骤 | 电压表读数 | |
| ⅰ.如图连接装置并加入试剂,闭合K | a | |
ⅱ.向B中滴入AgNO3(aq),至沉淀完全 | b | ||
ⅲ.再向B中投入一定量NaCl (s) | c | ||
ⅳ.重复ⅰ,再向B中加入与ⅲ等量NaCl(s) | a |
注:其他条件不变时,参与原电池反应的氧化剂(或还原剂)的氧化性(或还原性)越强,原电池的电压越大;离子的氧化性(或还原性)强弱与其浓度有关。
① 实验Ⅲ证明了AgCl转化为AgI,甲溶液可以是______(填序号)。
a. AgNO3溶液 b. NaCl溶液 c. KI溶液
② 实验Ⅳ的步骤ⅰ中,B中石墨上的电极反应式是______。
③ 结合信息,解释实验Ⅳ中b<a的原因:______。
④ 实验Ⅳ的现象能说明AgI转化为AgCl,理由是______。
(3)综合实验Ⅰ~Ⅳ,可得出结论: ______。