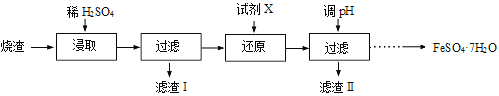
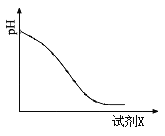
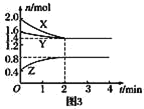
题目内容
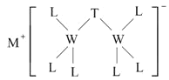
【题目】科学家合成出了一种新化合物(如图所示),其中M、W、T、L为同一短周期元素,L核外最外层电子数是W核外电子数的一半。下列叙述正确的是( )
A.化合物ML属于弱电解质
B.该新化合物中T满足8电子稳定结构
C.W的最高价氧化物可以与水反应生成弱酸
D.元素非金属性的顺序为W>T>L
【答案】B
【解析】
M、W、T、L为同一短周期元素,根据图知,W能形成4个共价键、L能形成1个共价键,则W位于第IVA族、L位于第VIIA族,且L核外最外层电子数是W核外电子数的一半,L最外层7个电子,则W原子核外有14个电子,故W为Si元素,L为Cl元素;该阴离子中Cl元素为-1价、W元素为+4价,根据化合价的代数和为-1价可知,T为-3价,所以T为P元素;根据阳离子所带电荷知,M为Na元素,据此解答。
通过以上分析知:M、W、T、L分别为Na、Si、P、Cl元素。
A. NaCl为离子化合物,但属于强电解质,故A错误;
B. 结合分析可知,该化合物中P为3价,P原子最外层电子数为5+3=8,满足8电子稳定结构,故B正确;
C. Si的最高价氧化物为SiO2,SiO2不与水反应,故C错误;
D. 同一周期元素非金属性随着原子序数增大而增强,则非金属性Cl>P>Si,即非金属性:L>T>W,故D错误;
故答案选:B。

【题目】下列有关实验的仪器选择和部分实验操作均正确的是( )
选项 | 实验 | 所选主要仪器铁架台等忽略 | 部分操作 |
A | 用浓硫酸配制480mL0.1mol/L硫酸溶液 | 500mL容量瓶、烧杯、玻璃棒、量筒、胶头滴管 | 将刚稀释所得的硫酸溶液立刻转移至500mL容量瓶,并加水至刻度线即可 |
B | 从食盐水中得到NaCl晶体 | 坩埚、酒精灯、玻璃棒、泥三角、三脚架 | 当加热至大量晶体出现时,停止加热,利用余热继续蒸干 |
C | 从碘的四氯化碳溶液中得到碘 | 蒸馏烧瓶、酒精灯、温度计、冷凝管、锥形瓶、牛角管 | 温度计水银球插入液液面以下 |
D | 用汽油提取溴水中的Br2 | 分液漏斗、烧杯 | 分离时下层液体从分液漏斗下口放出,上层液体从上口倒出 |
A.AB.BC.CD.D