题目内容
10.向NaCl、NaBr、NaI的混合溶液中通入Cl2后,若溶液中含有Br2,则一定不含有( )| A. | Cl2 | B. | I- | C. | Br- | D. | Cl- |
分析 卤素单质氧化性强弱顺序是Cl2>Br2>I2,所以氯气能氧化溴离子、碘离子,溴能氧化碘离子,据此判断溶液中存在微粒.
解答 解:卤素单质氧化性强弱顺序是Cl2>Br2>I2,所以氯气能氧化溴离子、碘离子,溴能氧化碘离子,混合溶液中含有Br2,溶液中可能含有Cl2、Br-,一定含有Cl-,因为碘离子能被溴氧化,所以一定不含碘离子,故选B.
点评 本题考查氧化还原反应,明确卤素单质氧化性强弱顺序是解本题关键,知道离子反应先后顺序,题目难度不大.

练习册系列答案
相关题目
20.锌与100mL 18.5mol•L-1的浓硫酸充分反应后,锌完全溶解,同时生成气体甲33.6L(标准状况).将反应后的溶液稀释至1L,测得溶液的pH=1.下列叙述正确的是.( )
| A. | 反应中共消耗1.85 mol H2SO4 | B. | 气体甲中SO2与H2的体积比为1:4 | ||
| C. | 反应中共消耗65 g Zn | D. | 反应中共转移3.6 mol电子 |
1.下列叙述中,不能用平衡移动原理解释的是( )
| A. | 由H2(g)、I2(g)、HI(g)组成的平衡体系加压后颜色变深 | |
| B. | 红棕色的NO2,加压后颜色先变深后变浅 | |
| C. | 实验室用排饱和食盐水法收集氯气 | |
| D. | 工业上利用O2与SO2反应制取SO3时通入过量O2 |
15.将一定量的Cu(OH)2和CuO的混合物投入2 L 1mol•L-1的盐酸中完全反应后.固体与盐酸均无剩余,则另取等质量的该混合物,用酒精灯加热,充分反应后所得固体的质量为( )
| A. | 80g | B. | 160g | C. | 98g | D. | 无法确定 |
2.下列反应中,放出气体的物质的量最多的是( )
| A. | 0.1mol Fe与足量的盐酸反应 | B. | 0.4mol Cu投入到足量的稀硫酸中 | ||
| C. | 0.1mol Al与足量的NaOH溶液反应 | D. | 0.1mol Fe与足量的水反应 |
16.如图是NaCl、MgSO4的溶解度曲线.下列说法正确的是( )
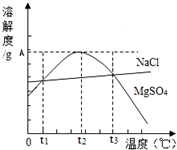

| A. | 只有在t1℃时,NaCl和MgSO4的溶解度才相等 | |
| B. | t1℃~t2℃,MgSO4的溶解度随温度升高而减小 | |
| C. | 在t2℃时,MgSO4饱和溶液的溶质质量分数最大 | |
| D. | 把MgSO4饱和溶液的温度从t3℃降至t2℃时,有晶体析出 |
 已知水在25℃和95℃时的电离平衡曲线如下图所示:
已知水在25℃和95℃时的电离平衡曲线如下图所示: