题目内容
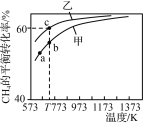
【题目】甲、乙为两个容积均为1 L的恒容密闭容器,向甲中充入1 mol CH4和1 mol CO2,乙中充入1 mol CH4和m mol CO2,加入催化剂,只发生反应:CH4(g)+CO2(g)![]() 2CO(g)+2H2(g),测得CH4的平衡转化率随温度的变化如图所示。下列说法正确的是( )
2CO(g)+2H2(g),测得CH4的平衡转化率随温度的变化如图所示。下列说法正确的是( )
A.该反应的正反应是放热反应
B.a、b、c三点处,容器内气体总压强:p(a)<p(b)<p(c)
C.T K时,该反应的平衡常数小于12.96
D.恒温时向甲的平衡体系中再充入CO2、CH4各0.4 mol,CO、H2各1.2 mol,重新达平衡前,v(正)>v(逆)
【答案】BC
【解析】
A. CH4的平衡转化率随温度的升高而升高,平衡正向移动,该反应的正反应是吸热反应,故A错误;
B. a、b温度升高,平衡正向移动,压强增大,p(a)<p(b);b、c,c的CH4的平衡转化率高,说明充入了更多的CO2,压强p(b)<p(c),a、b、c三点处,容器内气体总压强:p(a)<p(b)<p(c),故B正确;
C. T K时,假设甲的甲烷的转化率为60%,先算出平衡常数,
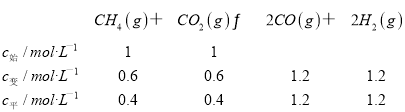
T K时,K=![]() =12.96,平衡时甲的甲烷的转化率小于60%,,该反应的平衡常数小于12.96,故C正确;
=12.96,平衡时甲的甲烷的转化率小于60%,,该反应的平衡常数小于12.96,故C正确;
D. Qc=![]() =12.96>K,恒温时向甲的平衡体系中再充入CO2、CH4各0.4 mol,CO、H2各1.2 mol,重新达平衡前,v(正)<v(逆),故D错误;
=12.96>K,恒温时向甲的平衡体系中再充入CO2、CH4各0.4 mol,CO、H2各1.2 mol,重新达平衡前,v(正)<v(逆),故D错误;
故选BC。

练习册系列答案
相关题目