题目内容
将4molA气体和2molB气体在2L的密闭容器中混合,并在一定条件下发生如下反应:2A(g)+B(g)?2C(g),反应2s后测得C的浓度为0.6mol/L.下列说法正确的是( )
| A.用物质A表示2s内的平均反应速率为0.3mol/(L?s) |
| B.用物质B表示2 s内的平均反应速率为0.6mol/(L?s) |
| C.2s后物质A的转化率为70% |
| D.2s后物质B的浓度为0.35mol/L |
反应2s后测得C的浓度为0.6mol/L,物质的量=0.6mol/L×2L=1.2mol;
2A(g)+B(g)?2C(g)
起始量(mol) 4 2 0
变化量(mol)1.20.61.2
2s末量(mol)2.81.41.2
A、用物质A表示2 s内的平均反应速率=
=0.3 mol/(L?s),故A正确;
B、用物质B表示2 s内的平均反应速率=
=0.15 mol/(L?s)故B错误;
C、2 s后物质A的转化率=
×100%=30%,故C错误;
D、2 s后物质B的浓度=
=0.7mol/L,故D错误;
故选A.
2A(g)+B(g)?2C(g)
起始量(mol) 4 2 0
变化量(mol)1.20.61.2
2s末量(mol)2.81.41.2
A、用物质A表示2 s内的平均反应速率=
| ||
| 2s |
B、用物质B表示2 s内的平均反应速率=
| ||
| 2s |
C、2 s后物质A的转化率=
| 1.2mol |
| 4mol |
D、2 s后物质B的浓度=
| 1.4mol |
| 2L |
故选A.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
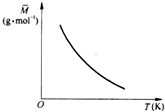
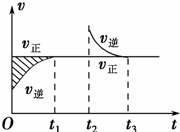
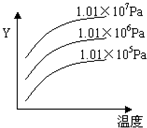
 2Z(g) △H<0,一段时间后达到平衡,反应过程中测定的数据如下表:
2Z(g) △H<0,一段时间后达到平衡,反应过程中测定的数据如下表: