题目内容
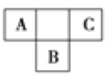
【题目】短周期元素A、B、C在元素周期表中的位置如图所示,已知A、B、C三种元素的原子核外电子数之和等于B的质子数的2倍。据此回答下列问题:
(1)A的气态氢化物的化学式为_________。
(2)B的元素符号为__________,在周期表中位于___________________。
(3)C的单质的化学式为__________,其氢化物的水溶液可用于雕刻玻璃。
【答案】NH3 S 三、ⅥA F2
【解析】
由短周期元素A、B、C在元素周期表中的位置,设B元素的质子数为x,则A的质子数为x-9,C的质子数为x-7,A、B、C三种元素的原子核外电子数之和等于B的质子数的2倍,则x-9+x+x-7=2x,解得x=16,则A为N元素、B为S元素、C为F元素,以此来解答。
根据上述分析可知,A为N元素,B为S元素,C为F元素。
(1)A是N元素,N原子最外层有5个电子,与3个H原子形成3对共用电子对,使每个原子都达到稳定结构,所以N的气态氢化物的化学式为NH3;
(2)B是硫元素,该元素的元素符号为S,原子核外电子排布为2、8、6,因此S元素在周期表中位于第三周期第VIA族;
(3)C元素是F,原子最外层有7个电子,因此2个F原子形成1对共用电子对,使每个原子都达到最外层8个电子的稳定结构,其单质的化学式为F2,该元素氢化物的水溶液氢氟酸能够与玻璃的成分二氧化硅发生反应,因此常用于雕刻玻璃。

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目



