题目内容
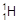 、
、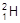 、
、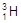 、H+、H2可以表示 ( )
、H+、H2可以表示 ( )| A.氢的五种同位素 | B.五种氢元素 |
| C.化学性质不同的氢原子 | D.氢元素的五种不同粒子 |
D
H2是单质。不是核素,所以选项D正确,答案选D。

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案
相关题目
题目内容
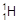 、
、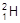 、
、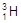 、H+、H2可以表示 ( )
、H+、H2可以表示 ( )| A.氢的五种同位素 | B.五种氢元素 |
| C.化学性质不同的氢原子 | D.氢元素的五种不同粒子 |

 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案