题目内容
下列解释事实的反应方程式正确的是
A.氨水使酚酞溶液变红:NH4+ + H2O NH3·H2O + H+ NH3·H2O + H+ |
| B.向FeCl3溶液中加入Mg(OH)2,溶液中有红褐色沉淀生成:3Mg(OH)2+2Fe3+=2Fe(OH)3+3Mg2+ |
| C.铅蓄电池放电时的正极反应为:PbO2+2e–+4H+=Pb2++2H2O |
| D.钢铁的析氢腐蚀与吸氧腐蚀的负极电极反应相同:Fe-3e–=Fe3+ |
B
解析试题分析:A、氨水是弱碱,电离出OH-,使酚酞溶液变红,电离方程式为NH3·H2O NH4+ + OH-,A不正确;B、由于氢氧化铁的溶度积常数小于氢氧化镁的溶度积常数,所以氢氧化镁能转化为氢氧化铁沉淀,即向FeCl3溶液中加入Mg(OH)2,溶液中有红褐色沉淀生成:3Mg(OH)2+2Fe3+=2Fe(OH)3+3Mg2+,B正确;C、铅蓄电池放电时的正极反应为:PbO2+2e–+SO42-+4H+=Pb SO4+2H2O,C不正确;D、钢铁的析氢腐蚀与吸氧腐蚀的负极电极反应相同:Fe-2e–=Fe2+,D不正确,答案选B。
NH4+ + OH-,A不正确;B、由于氢氧化铁的溶度积常数小于氢氧化镁的溶度积常数,所以氢氧化镁能转化为氢氧化铁沉淀,即向FeCl3溶液中加入Mg(OH)2,溶液中有红褐色沉淀生成:3Mg(OH)2+2Fe3+=2Fe(OH)3+3Mg2+,B正确;C、铅蓄电池放电时的正极反应为:PbO2+2e–+SO42-+4H+=Pb SO4+2H2O,C不正确;D、钢铁的析氢腐蚀与吸氧腐蚀的负极电极反应相同:Fe-2e–=Fe2+,D不正确,答案选B。
考点:考查电离方程式、电极反应式以及溶解平衡的有关判断

练习册系列答案
相关题目
下列事实中不能证明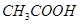 是弱电解质的是
是弱电解质的是
A.常温下某 |
B.常温下0.1mol 溶液的pH=2.8 溶液的pH=2.8 |
C. 溶液与稀盐酸反应生成 溶液与稀盐酸反应生成 |
D.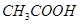 属于共价化合物 属于共价化合物 |
下列有关电解质溶液中微粒的物质的量浓度关系正确的是
| A.0.1 mol·L-1的NH4Cl溶液中:c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
| B.将醋酸钠、盐酸两溶液混合后,溶液呈中性,则混合后的溶液中:c(Na+)>c(Cl-) |
| C.已知Ka(HF)=7.2×10-4,Ka(HCN)=6.2×10-10,等体积等浓度的NaF、NaCN溶液中,前者离子总数小于后者 |
| D.浓度均为0.1 mol·L-1的①(NH4)2CO3②(NH4)2SO4③(NH4)2Fe(SO4)2溶液中,c(NH4+)的大小顺序为:③>②>① |
常温下,将0.1 mol·L-1氢氧化钠溶液与0.06 mol·L-1硫酸溶液等体积混合,该混合溶液的pH等于
| A.1.7 | B.2.0 | C.12.0 | D.12.4 |
物质的量浓度相同的下列溶液中,符合按pH由小到大的顺序排列的是
| A.Na2CO3 NaHCO3 NaCl NH4Cl | B.Na2CO3 NaHCO3 NH4Cl NaCl |
| C.(NH4)2SO4 NH4Cl NaNO3 Na2S | D.NH4Cl (NH4)2SO4 Na2S NaNO3 |
下列能正确表示水解的离子方程式是
A.CH3COOH + H2O  CH3COO- + H3O+ CH3COO- + H3O+ |
B.Br- + H2O  HBr + OH- HBr + OH- |
C.CO32- + 2H2O H2CO3 + 2OH- H2CO3 + 2OH- |
D.NH4+ + H2O  NH3·H2O + H+ NH3·H2O + H+ |