��Ŀ����
����Ŀ�����ǵؿ��з����ߵ�ϡ��Ԫ�أ��������������Ͻ����Ӽ���Ҳ������ҽҩ���Ƹ��������֯�ȹ�ҵ����̼������Ҫ��ѧ�ɷ�ΪCeFCO3��������ȡ�����Ҫ����ԭ�ϡ���̼����ұ�����������Ѿ���չ��ʮ���֣�����һ����ȡ��Ĺ�����������ͼ��ʾ��

��֪:���պ������к�+4�۵��漰ʮ3�۵�����ϡ��������������
��ش��������⣺
(1)CeFCO3��CeԪ�صĻ��ϼ�Ϊ______��
(2)�����ա�ǰ����ʯ�����ϸ������Ŀ����___________________________________________��
(3)�����I��������CeO2ת��ΪCe3+���Ҳ�������ɫ���壬�ù��̵����ӷ���ʽΪ___________________��
(4)�����1��������CeF4ת��Ϊ������Ce(BF4)3����������Լ��ε�Ŀ����__________________��
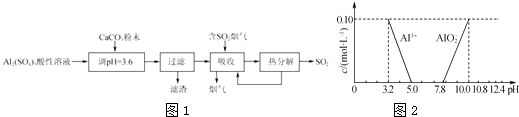
(5)������I��������Һ�м���NaOH��Һ��������ҺpH�ɻ��Ce(OH)3����������pH��ֽ�ⶨ��ҺpHֵ��ʵ�������__________________________________������Һ������Ũ��С��1��10-6mol/Lʱ��Ϊ������ȫ�������£�����NaOH������Һ��pHӦ����____[��֪Ce(OH)3��Ksp=8.0��10-21��1g2=0.3]��
(6)д��������������Ļ�ѧ����ʽ:_________________________________________��
���𰸡� +3 �������������ĽӴ�������ӿ췴Ӧ���ʣ����ԭ�ϵ������� 2CeO2+2Cl-+8H+=2Ce3++Cl2��+4H2O ����ʮ3������Ce(BF4)3��������ʽ��ʧ ȡһ��pH��ֽ���ڸ���ྻ�ı������ϣ��ò�����պȡ����Һ����pH��ֽ�����룬Ȼ�������ɫ������ 9.3 2Ce(OH)3+NaClO+H2O==2Ce(OH)4+NaCl
����������1���������и�Ԫ�ػ��ϼ�֮��Ϊ0��CeFCO3��Ce�Ļ��ϼ�Ϊx����x+��-1��+��+4��+��-2����3=0��x=+3����Ϊ�� +3
��2�����ڹ���μӵķ�Ӧ��˵����������Խ��Ӧ����Խ���������ա�ǰ����ʯ�����ϸ���������������������Ϊ���������������ĽӴ�������ӿ췴Ӧ���ʣ����ԭ�ϵ�������
��3�������������У����I�л������������ɫ���壬˵��Ce4+ ���Ӿ���ǿ�����ԣ��ɽ�Cl- ����ΪCl2 �����ӷ���ʽΪ��2CeO2+2Cl-+8H+=2Ce3++Cl2��+4H2O����Ϊ��2CeO2+2Cl-+8H+=2Ce3++Cl2��+4H2O��
��4��+3������������������Ce(BF4)3,��������Լ��οɱ���+3��������Ce(BF4)3������Ӷ�����CeԪ�ص���ģ���Ϊ������+3������Ce(BF4)3��������ʽ��ʧ.
��5��ʵ���ҲⶨPH�ķ�����˺��һСƬpH��ֽ���ڸ���ྻ�ı�������,�ò�����պȡ����Һ����pH��ֽ������,Ȼ�������ɫ���Ա�������Һ������Ũ��С��![]() ʱ��Ϊ������ȫ,����ܶȻ�������������������Ũ��
ʱ��Ϊ������ȫ,����ܶȻ�������������������Ũ��![]() ,
,![]() ,�õ���Һ
,�õ���Һ![]() ,��Ϊ��ȡһ��pH��ֽ���ڸ���ྻ�ı������ϣ��ò�����պȡ����Һ����pH��ֽ�����룬Ȼ�������ɫ������ ��9.3.
,��Ϊ��ȡһ��pH��ֽ���ڸ���ྻ�ı������ϣ��ò�����պȡ����Һ����pH��ֽ�����룬Ȼ�������ɫ������ ��9.3.
(6)NaClO��Ce(OH)3����ΪCe(OH)4,����NaClΪ��ԭ����,��Ϊ:2Ce(OH)3+NaClO+H2O=2Ce(OH)4+NaCl

 ��ְٷְټ�����Ԫ��ĩ���Ծ�ϵ�д�
��ְٷְټ�����Ԫ��ĩ���Ծ�ϵ�д� Сѧ��ĩ���Ծ�ϵ�д�
Сѧ��ĩ���Ծ�ϵ�д�����Ŀ��I.ij��ѧ��Ӧ�У���Ӧ�����A��B��C�����ʵ���Ũ��(c)��ʱ��(t)�Ĺ�ϵ���±���ʾ��
��ʼ | 2 min | 4 min | 6 min | |
c(A)/mol��L��1 | 1.45 | 1.28 | 1.00 | 1.00 |
c(B)/mol��L��1 | 0.38 | 0.72 | 1.28 | 1.28 |
c(C)/mol��L��1 | 0.095 | 0.18 | 0.32 | 0.32 |
��1�� �÷�Ӧ�Ļ�ѧ����ʽΪ __________________________________
��2��4 minĩA��ת����ԼΪ______________
II��ij̽����ѧϰС������ͬ������п����ͬŨ�ȵ�������ϡ���ᷴӦ�õ�ʵ�����������ʾ��
ʵ���� | п����̬ | ��Ӧ�¶�/�� | �ռ�100 mL��������ʱ��/s |
�� | ��Ƭ | 15 | 200 |
�� | ��Ƭ | 25 | 90 |
�� | ��ĩ | 25 | 10 |
(3)��ʵ���Ŀ����̽��________��________��п��ϡ���ᷴӦ���ʵ�Ӱ�졣
(4)ʵ���͢����________����ѧ��Ӧ����Խ��
(5)�ܱ�������ı�����Է�Ӧ������Ӱ���ʵ������________��________��
(6)�����һ��ʵ�鷽��֤�������Ũ�ȶԸ÷�Ӧ�����ʵ�Ӱ�죺___________________��