题目内容
1.在酸碱中和滴定中,取用20.00mL的NaOH溶液应该使用( )| A. | 烧杯 | B. | 天平 | C. | 酸式滴定管 | D. | 碱式滴定管 |
分析 滴定管精确到0.01,氢氧化钠溶液呈碱性,应用碱式滴定管,据此解题.
解答 解:烧杯一般做反应容器,天平一般用来称量物体,滴定管精确到0.01,氢氧化钠溶液呈碱性,应用碱式滴定管.
故选D.
点评 本题考查常见仪器的使用和化学基本操作的方法,题目难度不大,注意在学习中加强基础知识的积累.

练习册系列答案
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案
相关题目
9.设NA代表阿伏加德罗常数的值,下列说法正确的是( )
| A. | 常温常压下,11.2 L氧气所含的氧原子数为NA | |
| B. | 1 mol/L的CaCl2溶液中含有的Cl-为2 NA | |
| C. | 2.4 g镁变成Mg2+时失去的电子数目为0.2 NA | |
| D. | 标准状况下,2 g氢气所含的原子数目为NA |
16.2011年3月11日的日本大地震造成日本福岛核电站出现严重事故,由核反应堆泄漏出的${\;}_{53}^{131}$I和罗${\;}_{55}^{137}$Cs引起了全世界的关注,其中${\;}_{55}^{137}$Cs原子核内的中子数为( )
| A. | 82 | B. | 55 | C. | 137 | D. | 192 |
6.某温度下,反应2N2O5?4NO2+O2开始进行时,c(N2O5)=0.040 8mol/L.经1min后,c(N2O5)=0.030mol/L.则该反应的反应速率为( )
| A. | v(N2O5)=1.8×10-4 mol/(L•s) | B. | v(N2O5)=1.08×10-2 mol/(L•s) | ||
| C. | v(NO2)=1.8×104 mol/(L•s) | D. | v(O2)=1.8×104 mol/(L•s) |
10.下列化学方程式中,书写完全正确的是( )
| A. | 2H2O=2H2↑+O2↑ | B. | H2SO4+NaOH=NaSO4+H2O | ||
| C. | Fe+HCI=FeCI2+H2↑ | D. | 2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑ |
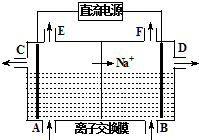 电解原理在工业生产中有广泛的应用.
电解原理在工业生产中有广泛的应用.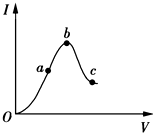 在一定温度下,将冰醋酸加水稀释的过程中,溶液的导电能力I随加入水的体积V变化的曲线如图所示.
在一定温度下,将冰醋酸加水稀释的过程中,溶液的导电能力I随加入水的体积V变化的曲线如图所示.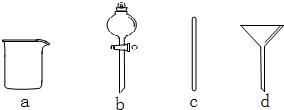 实验室需要0.1mol•L-1NaOH溶液480mL.根据溶液的配制情况回答下列问题.
实验室需要0.1mol•L-1NaOH溶液480mL.根据溶液的配制情况回答下列问题.