题目内容
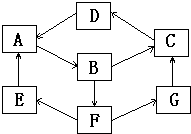
A、B、C分别是三种常见金属单质,其中B的氧化物和氢氧化物都是两性化合物.A、B、C和气体甲、乙、丙及物质D、E、F、G、H,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出).

请根据以上信息回答下列问题:
(1)写出下列物质的化学式:D______、乙______
(2)在反应①~⑥中,不属于氧化还原反应的是______
(3)写出下列反应离子方程式:
反应①:______
反应③:______
气体乙与D物质溶液反应:______
(4)若在F物质溶液中加入D物质溶液,能观察到的现象是______,发生反应的化学方程式为______、______.

请根据以上信息回答下列问题:
(1)写出下列物质的化学式:D______、乙______
(2)在反应①~⑥中,不属于氧化还原反应的是______
(3)写出下列反应离子方程式:
反应①:______
反应③:______
气体乙与D物质溶液反应:______
(4)若在F物质溶液中加入D物质溶液,能观察到的现象是______,发生反应的化学方程式为______、______.
金属单质A的焰色反应为黄色,应为Na,与水反应生成的气体甲为H2,D为NaOH,黄绿色气体乙为Cl2,则丙为HCl,E为盐酸,能与NaOH反应生成氢气的B为Al,红褐色沉淀H为Fe(OH)3,则C为Fe,F为FeCl2 ,G为FeCl3,
(1)由以上分析可知D为NaOH,乙为Cl2,故答案为:NaOH;Cl2;
(2)①为钠与水的反应,为氧化还原反应,②为氯气和氢气的化合反应,为氧化还原反应,③为铝和氢氧化钠溶液生成氢气的反应,为氧化还原反应,
④为铁和盐酸置换氢气的反应,为氧化还原反应,⑤为氯气和氯化亚铁的反应,为氧化还原反应,⑥氢氧化钠与氯化铁的复分解反应,不是氧化还原反应,
故答案为:⑥;
(3)①为钠与水的反应,生成氢氧化钠和氢气,反应的方程式为2Na+2H2O=2Na++2OH-+H2↑,
③为铝和氢氧化钠溶液生成氢气的反应,方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑,
氯气与氢氧化钠反应生成氯化钠、次氯酸钠和水,反应的离子方程式为Cl2+2OH-=Cl-+ClO-+H2O,
故答案为:2Na+2H2O=2Na++2OH-+H2↑;2Al+2OH-+2H2O=2AlO2-+3H2↑;Cl2+2OH-=Cl-+ClO-+H2O;
(4)氯化亚铁与氢氧化钠反应生成白色氢氧化亚铁沉淀,氢氧化亚铁不稳定,易被空气中氧气氧化生成氢氧化铁,可观察到白色沉淀逐渐变成灰绿色,最终变成红褐色,
反应的方程式为FeCl2+2NaOH=Fe(OH)2↓+2NaCl、4Fe(OH)2+O2+2H2O=4Fe(OH)3,
故答案为:产生白色沉淀,逐渐变成灰绿色,最终变成红褐色;FeCl2+2NaOH=Fe(OH)2↓+2NaCl;4Fe(OH)2+O2+2H2O=4Fe(OH)3.
(1)由以上分析可知D为NaOH,乙为Cl2,故答案为:NaOH;Cl2;
(2)①为钠与水的反应,为氧化还原反应,②为氯气和氢气的化合反应,为氧化还原反应,③为铝和氢氧化钠溶液生成氢气的反应,为氧化还原反应,
④为铁和盐酸置换氢气的反应,为氧化还原反应,⑤为氯气和氯化亚铁的反应,为氧化还原反应,⑥氢氧化钠与氯化铁的复分解反应,不是氧化还原反应,
故答案为:⑥;
(3)①为钠与水的反应,生成氢氧化钠和氢气,反应的方程式为2Na+2H2O=2Na++2OH-+H2↑,
③为铝和氢氧化钠溶液生成氢气的反应,方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑,
氯气与氢氧化钠反应生成氯化钠、次氯酸钠和水,反应的离子方程式为Cl2+2OH-=Cl-+ClO-+H2O,
故答案为:2Na+2H2O=2Na++2OH-+H2↑;2Al+2OH-+2H2O=2AlO2-+3H2↑;Cl2+2OH-=Cl-+ClO-+H2O;
(4)氯化亚铁与氢氧化钠反应生成白色氢氧化亚铁沉淀,氢氧化亚铁不稳定,易被空气中氧气氧化生成氢氧化铁,可观察到白色沉淀逐渐变成灰绿色,最终变成红褐色,
反应的方程式为FeCl2+2NaOH=Fe(OH)2↓+2NaCl、4Fe(OH)2+O2+2H2O=4Fe(OH)3,
故答案为:产生白色沉淀,逐渐变成灰绿色,最终变成红褐色;FeCl2+2NaOH=Fe(OH)2↓+2NaCl;4Fe(OH)2+O2+2H2O=4Fe(OH)3.

练习册系列答案
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目

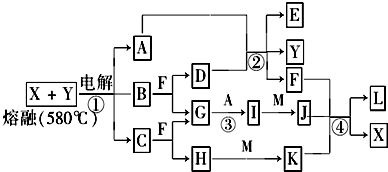
 (2)如果C是液态物质:①写出A的电极反应方程式:阴极 ;阳极 ;②写出H I的化学方程式 ;③G与足量Cl2反应的离子方程式 。
(2)如果C是液态物质:①写出A的电极反应方程式:阴极 ;阳极 ;②写出H I的化学方程式 ;③G与足量Cl2反应的离子方程式 。