题目内容
1.下列分子中所有原子都满足最外层为8个电子结构的是( )| A. | BF3 | B. | CCl4 | C. | H2O | D. | PCl5 |
分析 对于ABn型共价化合物元素化合价绝对值+元素原子的最外层电子层=8,则该元素原子满足8电子结构,据此判断.
解答 解:A、BF3中B元素化合价为+3,B原子最外层电子数为3,所以3+3=6,B原子不满足8电子结构;F元素化合价为-1,F原子最外层电子数为7,所以1+7=8,F原子满足8电子结构,故A错误;
B、CCl4中C元素化合价为+4,C原子最外层电子数为4,所以4+4=8,C原子满足8电子结构;Cl元素化合价为-1,Cl原子最外层电子数为7,所以1+7=8,Cl原子满足8电子结构,故B正确;
C、H2O中O元素化合价为-2,O原子最外层电子数为6,所以2+6=8,O原子满足8电子结构;H元素化合价为+1,H原子最外层电子数为1,所以1+1=2,H原子不满足8电子结构,故C错误;
D、PCl5中P元素化合价为+5,P原子最外层电子数为5,所以5+5=10,P原子不满足8电子结构;Cl元素化合价为-1,Cl原子最外层电子数为7,所以1+7=8,Cl原子满足8电子结构,故D错误;
故选B.
点评 本题考查8电子结构的判断,难度不大,清楚元素化合价绝对值+元素原子的最外层电子层=8,则该元素原子满足8电子结构是关键,注意离子化合物不适合.

练习册系列答案
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案
相关题目
11.某烷烃分子中含有手性碳原子,该烷烃分子中的碳原子数至少为( )
| A. | 5 | B. | 6 | C. | 7 | D. | 8 |
12.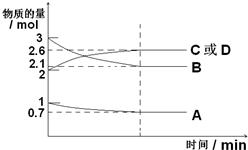 在一定温度下某密闭容器中,加入1moA、3molB、2molC和2molD,发生反应:m A(g)+n B(g)?x C(g)+y D(s),各物质的物质的量随着时间的变化如图所示,则当下列条件成立时,能说明反应已经达到平衡状态的是( )
在一定温度下某密闭容器中,加入1moA、3molB、2molC和2molD,发生反应:m A(g)+n B(g)?x C(g)+y D(s),各物质的物质的量随着时间的变化如图所示,则当下列条件成立时,能说明反应已经达到平衡状态的是( )
①C的生成速率与C的分解速率相等
②ひ正(A)=2ひ逆(C)
③A、B、C的浓度不再变化
④反应物的转化率不再变化
⑤混合气体的压强不再变化
⑥混合气体的物质的量不再变化
⑦单位时间内消耗amolA,同时生成 3amolB
⑧A、B、C、D的分子数之比为1:3:2:2.
 在一定温度下某密闭容器中,加入1moA、3molB、2molC和2molD,发生反应:m A(g)+n B(g)?x C(g)+y D(s),各物质的物质的量随着时间的变化如图所示,则当下列条件成立时,能说明反应已经达到平衡状态的是( )
在一定温度下某密闭容器中,加入1moA、3molB、2molC和2molD,发生反应:m A(g)+n B(g)?x C(g)+y D(s),各物质的物质的量随着时间的变化如图所示,则当下列条件成立时,能说明反应已经达到平衡状态的是( )①C的生成速率与C的分解速率相等
②ひ正(A)=2ひ逆(C)
③A、B、C的浓度不再变化
④反应物的转化率不再变化
⑤混合气体的压强不再变化
⑥混合气体的物质的量不再变化
⑦单位时间内消耗amolA,同时生成 3amolB
⑧A、B、C、D的分子数之比为1:3:2:2.
| A. | ①②③④⑤⑥⑦ | B. | ①③④⑤⑥⑦ | C. | ①③④⑥⑦ | D. | ①③⑤⑥⑦⑧ |
9.已知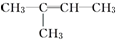 的键线式可写作
的键线式可写作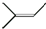 ,某有机物的键线式为
,某有机物的键线式为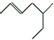 ,其正确名称是( )
,其正确名称是( )
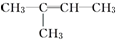 的键线式可写作
的键线式可写作 ,某有机物的键线式为
,某有机物的键线式为 ,其正确名称是( )
,其正确名称是( )| A. | 5-乙基-2-己烯 | B. | 2-甲基庚烯 | C. | 3-甲基-5-庚烯 | D. | 5-甲基-2-庚烯 |
16.下列不能用作喷泉实验的组合的是( )
| A. | HCl和水 | B. | 氨气和稀硫酸 | ||
| C. | 氯气和饱和食盐水 | D. | CO2和NaOH溶液 |
13.食品安全已是百姓最关心的问题之一,食品在油炸过程中会产生一种不利于人体健康的物质CH2=CH-CO-NH2(丙烯酰胺),对这种物质的叙述不正确的是( )
| A. | 能发生加聚反应生成高分子化合物 | B. | 该物质与HCl加成产物只一种 | ||
| C. | 具有多种同分异构体 | D. | 可与强酸反应 |
10.写出下列分子中中心原子的杂化方式与分子空间构型
| 中心原子杂化方式 | 分子空间构型 | |
| NH3 | sp3 | 三角锥形 |
| BF3 | sp2 | 平面正三角形 |
| H2O | sp3 | V形 |
11.下列说法中,正确的是( )
| A. | CO2的摩尔质量为44g | |
| B. | 1molN2的质量是14g | |
| C. | 标准状况下,1molCO2所占的体积约是22.4L | |
| D. | 将40gNaOH溶于1L水中,所得溶液中NaOH的物质的量浓度为1mol/L |
