题目内容
8.化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的.如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化:下列说法中正确的是( )
| A. | 1 mol N2(g)和1 mol O2(g)反应放出的能量为180 kJ | |
| B. | 1 mol N2(g)和1 mol O2(g)具有的总能量小于2 mol NO(g)具有的总能量 | |
| C. | 1 mol N2(g)和1 mol O2(g)具有的总键量小于2 mol NO(g)具有的总键量 | |
| D. | 通常情况下,N2(g)和O2(g)混合能直接生成NO |
分析 焓变等于化学键断裂时吸收的能量减去化学键形成时放出的能量,则N2(g)+O2(g)=2NO(g)的焓变△H=946kJ/mol+498kJ/mol-2×632kJ/mol=+180kJ/mol,为吸热反应,以此来解答.
解答 解:A.焓变为正,则1 mol N2(g)和1 mol O2(g)反应吸收的能量为180 kJ,故A错误;
B.为吸热反应,则1 mol N2(g)和1 mol O2(g)具有的总能量小于2 mol NO(g)具有的总能量,故B正确;
C.为吸热反应,1 mol N2(g)和1 mol O2(g)具有的总键量大于2 mol NO(g)具有的总键量,故C错误;
D.通常情况下,N2(g)和O2(g)不反应,高温或放电时生成NO,故D错误;
故选B.
点评 本题考查反应热与焓变,为高频考点,把握反应中能量变化、焓变与键能或总能量的关系为解答的关键,侧重分析与应用能力的考查,注意选项A为易错点,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
14.甲、乙两烧杯中各盛有100mL 6mol/L的盐酸和NaOH溶液,向两烧杯中分别加入等质量的铝粉,反应结束后测得生成的气体体积比为1:2,则加入铝粉的质量为( )
| A. | 10.8g | B. | 7.2g | C. | 5.4g | D. | 3.6g |
19.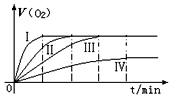 某实验小组以 H2O2分解为例,研究浓度、催化剂、温度对反应速率的影响.按照如下方案完成实验.通过实验得到氧气的体积与时间的关系如图所示,回答下列问题:
某实验小组以 H2O2分解为例,研究浓度、催化剂、温度对反应速率的影响.按照如下方案完成实验.通过实验得到氧气的体积与时间的关系如图所示,回答下列问题:
(1)代表实验①的图示是Ⅳ.
(2)对比实验③和④的目的是探究催化剂对反应速率的影响.
(3)通过上面对比实验,所得的实验结论是其他条件不变,增大反应物浓度或升高温度或加入催化剂,化学反应速率加快.
 某实验小组以 H2O2分解为例,研究浓度、催化剂、温度对反应速率的影响.按照如下方案完成实验.通过实验得到氧气的体积与时间的关系如图所示,回答下列问题:
某实验小组以 H2O2分解为例,研究浓度、催化剂、温度对反应速率的影响.按照如下方案完成实验.通过实验得到氧气的体积与时间的关系如图所示,回答下列问题:| 反应物 | 催化剂 | 温度 | |
| ① | 10mL10% H2O2溶液 | 无 | 25℃ |
| ② | 10mL20% H2O2溶液 | 无 | 25℃ |
| ③ | 10mL20% H2O2溶液 | 无 | 40℃ |
| ④ | 10mL20% H2O2溶液 | 1~2滴0.1mol/L FeCl3溶液 | 40℃ |
(2)对比实验③和④的目的是探究催化剂对反应速率的影响.
(3)通过上面对比实验,所得的实验结论是其他条件不变,增大反应物浓度或升高温度或加入催化剂,化学反应速率加快.
16.化学式为C5H12O的醇有( )种.
| A. | 8 | B. | 4 | C. | 2 | D. | 1 |
3.下列图示烷烃的二溴代物有( )


| A. | 2种 | B. | 4种 | C. | 6种 | D. | 8种 |
13.下列对NO、NO2的描述,正确的是( )
| A. | NO是红棕色气体,易溶于水,是酸性氧化物 | |
| B. | NO2可用排水法收集,且可由N2和O2化合而得到 | |
| C. | NO、NO2在一定条件下可相互转化,且二者都是引起光化学烟雾的大气污染物 | |
| D. | NO、NO2互为同素异形体,且NO是汽车尾气的有害成分之一 |
20.只用一种试剂就能将 、
、 、CH3CH2OH鉴别出来,该试剂是( )
、CH3CH2OH鉴别出来,该试剂是( )
 、
、 、CH3CH2OH鉴别出来,该试剂是( )
、CH3CH2OH鉴别出来,该试剂是( )| A. | 溴水 | B. | NaOH溶液 | C. | 饱和Na2CO3溶液 | D. | 银氨溶液 |
17.下列物质中,一定不是天然高分子化合物的是( )
| A. | 橡胶 | B. | 蛋白质 | C. | 油脂 | D. | 纤维素 |
18.下列溶液中,溶质的阴离子和阳离子的物质的量浓度相等的是( )
| A. | NaHSO3 | B. | CH3COONa | C. | NaCl | D. | MgSO4 |