题目内容
3.在复杂的体系中,确认化学反应先后顺序有利于解决问题,下列化学反应先后顺序判断不正确的是( )| A. | 在含Ba(OH)2、KOH的混合溶液中缓慢通入CO2:Ba(OH)2、KOH、K2CO3、BaCO3 | |
| B. | 在含NH4+、Al3+、H+的溶液中逐滴加入KOH溶液:H+、Al3+、NH4+、Al(OH)3 | |
| C. | 在含AlO2-、OH-、CO32-的溶液中逐滴加入盐酸:AlO2-、Al(OH)3、OH-、CO32- | |
| D. | 在含等物质的量的Fe2+、Ag+、Cu2+、H+的溶液中加入锌粉:Ag+、Cu2+、H+、Fe2+ |
分析 A.氢氧化钡先发生反应,因为碳酸钾与氢氧化钡不能共存;
B.氢离子优先反应,其次是铝离子反应生成氢氧化铝,然后铵根离子反应,最后氢氧化铝溶解;
C.用假设法判断,H+最先与AlO2-反应,生成氢氧化铝,而氢氧化铝与溶液中OH-反应生成AlO2-;
D.同一还原剂与不同具有氧化性的物质反应时,先与氧化性强的物质反应.
解答 解:A.含等物质的量的Ba(OH)2、KOH的溶液中通入CO2,氢氧化钡优先反应,反应的先后顺序为:Ba(OH)2、KOH、K2CO3、BaCO3,故A正确;
B.在含有NH4+、H+、Al3+ 的溶液中,逐滴加入NaOH溶液,氢离子优先反应,其次是铝离子反应生成氢氧化铝,然后铵根离子反应,最后氢氧化铝溶解,反应的先后顺序为:H+、Al3+、NH4+、Al(OH)3,故B正确;
C.含等物质的量的AlO2-、OH-、CO32-的溶液中,逐滴加入盐酸,氢氧根离子优先反应,反应的先后顺序为:OH-、AlO2-、CO32-、Al(OH)3,故C错误;
D.氧化性由大到小的顺序为Ag+、Cu2+、H+、Fe2+,含等物质的量的Fe2+、Ag+、Cu2+、H+的溶液中加入Zn,反应顺序为:Ag+、Cu2+、H+、Fe2+,故D正确;
故选C.
点评 本题考查了离子反应的先后顺序,题目难度中等,明确常见物质性质及离子反应发生条件为解答关键,试题侧重考查学生的分析、理解能力及灵活应用基础知识的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
13.设NA为阿伏加德罗常数的值.下列叙述不正确的是( )
| A. | 7.80g Na2O2与5.85g NaCl所含阴离子数均为0.1NA | |
| B. | 一定条件下,1.4g N2与0.2mol H2混合充分反应,转移的电子数为0.3NA | |
| C. | 常温常压下,22.4LNH3所含分子数小于NA | |
| D. | 标准状况下,28g聚乙烯完全燃烧,产生的CO2数为2NA |
14.在有机分子中,若某个碳原子连接着4个不同的原子或原子团,则这个碳原子被称为“手性碳原子”,凡含有手性碳原子的物质一定具有光学活性.下列物质中无光学活性的是( )
| A. | CH3CH(Br)OH | B. | CH3CH(CH2OH)CHO | ||
| C. | CH3CH2CH(CH3)CH2CH3 | D. | HOOCCH(Br)COOCH3 |
18.已知A、B、C、D、E是短周期中原子序数依次增大的5种元素,B、C同周期,D、E也同周期,D原子最外层电子数与最内层电子数相等,A、B、C、D的原子序数之和是E的两倍,D与C形成的化合物是一种耐高温材料,A、B形成的气态化合物的水溶液呈碱性.下列说法正确的是( )
| A. | 原子半径:D>E>C>B>A | |
| B. | 热稳定性:EA4>A2C | |
| C. | 单质D可用海水作原料获得 | |
| D. | 化合物DC与化合物EC2中化学键类型相同 |
8.下列物质能够使酸性高锰酸钾褪色的是( )
| A. | 苯 | B. | 乙酸 | C. | 乙烷 | D. | 油脂 |
15.电化学在日常生活中有广泛的应用,下列说法或做法正确的是( )
| A. | 暴雨后遭洪水浸泡的铁门生锈是因为发生化学腐蚀 | |
| B. | 白铁皮(铁镀锌)表面有划损时,不能阻止铁被腐蚀 | |
| C. | 废弃的干电池不能随意丢弃,但可以土埋处理 | |
| D. | 不能将铁制自来水管与铜制水龙头连接 |
13.在下列结构中,核磁共振氢谱中出现三组峰的化合物是( )
| A. |  | B. | 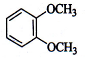 | C. | 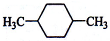 | D. |  |
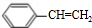 ,A分子中处于同一平面的原子最多有16个;
,A分子中处于同一平面的原子最多有16个;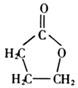 :
: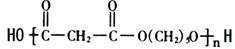 .
.