题目内容
下列说法正确的是
| A.在标准状况下,1mol水的体积是22.4L |
B.1mol 所占的体积一定是22.4L 所占的体积一定是22.4L |
C.1L0.5mol/L的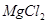 溶液中,含有 溶液中,含有 的个数为 的个数为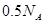 |
D.在标准状况下,总质量为28g的 和CO的混合气体,其体积约为22.4L 和CO的混合气体,其体积约为22.4L |
D
解析试题分析:A标准状况下,水是非气态,B不是在标准状况就不一定是22.4L,C中氯离子是NA。
考点:考查对气体摩尔体积和物质的量浓度的计算。D中28g恰好是1mol标况下为22.4L。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列有关化学用语表示正确的是( )
| A.3—甲基—1—丁烯的结构简式:(CH3)2CHCH=CH2 |
B.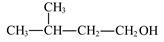 的名称是3-甲基丁醇 的名称是3-甲基丁醇 |
C.乙炔的分子结构模型示意图: |
D.CH4Si的结构式: |
某稀硫酸和稀硝酸的混合溶液200 mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解9.6 g。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示(已知硝酸只被还原为NO气体)。下列分析或结果错误的是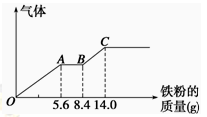
| A.原混合酸中NO3-物质的量为0.1 mol |
| B.OA段产生的是NO,AB段的反应为Fe+2Fe3+=3Fe2+,BC段产生氢气 |
| C.第二份溶液中最终溶质为FeSO4 |
| D.H2SO4浓度为2.5 mol·L-1 |
实验室需配制一种c (H+)=2mol/L的强酸溶液500mL,下列配制方法可行的是( )
| A.取100mL5mol/LH2SO4,加入400mL水 |
| B.取200mL5mol/LHCl,加水稀释至500mL |
| C.取200 mL5mol/LH2SO4,加水稀释至500mL |
| D.取100 mL5mol/LHNO3,加水稀释至500mL |
NA代表阿伏加德罗常数。下列有关叙述正确的是
| A.标准状况下,2.24 L H2O含有的分子数大于0.1NA |
| B.常温下,100 mL 1 mol/L Na2CO3溶液中阴离子总数小于0.1NA |
| C.分子数为NA的C2H4气体体积约为22.4 L |
| D.1.7 g NH3中含N—H键数目为0.1NA |
下列化学用语书写正确的是( )
A.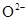 的离子结构示意图: 的离子结构示意图: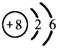 |
B.CH4分子的比例模型: |
C.四氯化碳的电子式: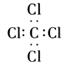 |
D.用电子式表示氯化氢分子的形成过程: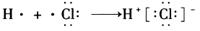 |
若阿伏加德罗常数的数值用NA表示,下列说法正确的是( )
| A.常温常压下,22.4L氯气与足量镁粉充分反应,转移的电子数为2NA |
| B.1.6gNH2-离子所含质子数为NA |
| C.50mL18.4mol·L—1浓硫酸与足量铜微热反应,生成SO2分子的数目为0.46NA |
| D.28g乙烯和环丁烷(C4H8)的混合气体中含有的碳原子数为2NA |
NA表示阿伏加德罗常数,以下各物质所含分子数最多的是( )
| A.标准状况下11.2 L氯气 | B.17g氨气 |
| C.0.8mol氧气 | D.4℃时,36mL的H2O |
用1L1mol·L-1NaOH溶液吸收0.8molCO2,所得溶液中Na2CO3和NaHCO3的物质的量之比约为( )
| A.1︰3 | B.1︰2 | C.2︰3 | D.3︰2 |