题目内容
如图是一个盐桥中充满饱和KCl溶液的锌铜原电池装置,下列分析正确的是
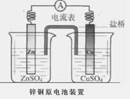

| A.Cu片上发生氧化反应 |
| B.电子由Cu片经外电路流向Zn片 |
| C.盐桥中的Cl―移向ZnSO4溶液 |
| D.一段时间后烧杯中c(Zn2+)、c(Cu2+)均减小 |
C
试题分析:装置中,形成原电池,锌为活泼金属,被氧化而失去电子,铜为原电池正极,正极上得电子而被还原,原电池中,电子由负极经外电路流向正极,电解质溶液中,阳离子向正极移动,阴离子向负极移动。A、铜为原电池正极,被还原,故A错误;B、原电池中电子由负极经外电路流向正极,故B错误;电解质溶液中阴离子向负极移动,故C正确;D、原电池,锌为活泼金属,被氧化而失去电子,铜为原电池正极,正极上得电子而被还原成铜离子,使溶液中锌离子浓度升高,铜离子浓度降低,故D错误。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
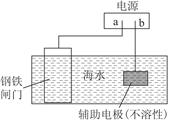
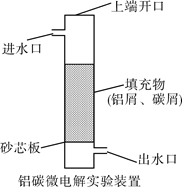

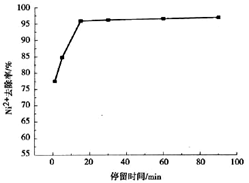


 Fe(OH)2+Ni(OH)2,下列对该蓄电池推断错误的是:
Fe(OH)2+Ni(OH)2,下列对该蓄电池推断错误的是: