题目内容
【题目】在A、B、C三个烧杯中分别盛有相同浓度的稀硫酸,如图所示:
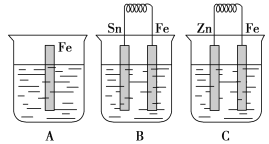
(1)A中反应的离子方程式为_____________________________。
(2)B中Sn极的电极反应式为____________________________,Sn极附近溶液的pH________(填“增大”“减小”或“不变”)。
(3)C中被腐蚀的金属是________,总反应的离子方程式为________________,比较A、B、C中铁被腐蚀的速率,由快到慢的顺序是________________。
【答案】(1)Fe+2H+=Fe2++H2↑
(2)2H++2e-=H2↑ 增大
(3)Zn Zn+2H+=Zn2++H2↑ B>A>C
【解析】(1)A中发生的是铁与稀硫酸直接发生的置换反应,反应的离子方程式为Fe+2H+=Fe2++H2↑。
(2)Fe比Sn活泼,B中Fe做负极,Sn做正极,H+在Sn极上放电,发生的电极反应式为2H++2e-=H2↑。Sn极附近溶液H+被消耗,则pH增大。
(3)Zn比Fe活泼,Zn做负极,失电子被氧化,则被腐蚀的金属是Zn,总反应的离子方程式为Zn+2H+=Zn2++H2↑。铁在不同的情况下被腐蚀的速率不同,作原电池的负极时易被腐蚀,作原电池的正极时受到保护不被腐蚀。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】无机化合物可根据其组成和性质进行分类,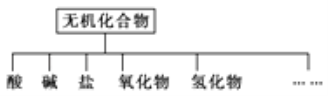
(1)如图所示的物质分类方法名称是 .
(2)如下表格
物质类别 | 酸 | 碱 | 盐 | 酸性 | 碱性 |
化学式 | ①② | ③④Ba(OH)2 | ⑤Na2CO3 | ⑦SO2 | ⑨﹣﹣ |
以Na、K,H,O,C,S,N中任两种或三种元素组成合适的物质,分别填在上表中①②③⑥⑧⑨⑩后面的横线上.
(3)写出少量的⑦通入NaOH溶液的化学方程式: .
(4)实验室制备⑦常用和反应,检验该气体的方法是
(5)写出④与⑤反应的离子方程式 .