题目内容
4.设NA代表阿伏加德罗常数的值,下列说法正确的是( )| A. | 常温常压下32g O2和O3所含的原子数为2NA | |
| B. | 标准状况下22.4L CCl4所含的分子数为NA | |
| C. | 1mol/L CaCl2溶液中所含的Cl-离子数为2NA | |
| D. | 56 g Fe与任何物质完全反应时转移的电子数一定为2NA |
分析 A、O2和O3均由氧原子构成;
B、标况下,四氯化碳为液体;
C、溶液体积不明确;
D、求出铁的物质的量,然后根据铁反应后的价态来分析.
解答 解:A、O2和O3均由氧原子构成,故32g混合物中含有的氧原子的物质的量n=$\frac{32g}{16g/mol}$=2mol,即2NA个,故A正确;
B、标况下,四氯化碳为液体,不能根据气体摩尔体积来计算其物质的量,故B错误;
C、溶液体积不明确,故溶液中的氯离子的个数不能计算,故C错误;
D、56g铁的物质的量为1mol,而铁反应后的价态可能变为+2价或+3价,故1mol铁失去的电子数可能为2NA个,也可能为3NA个,故D错误.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.

练习册系列答案
相关题目
14.维生素A的结构简图如图所示,关于它的叙述中正确的是( )


| A. | 维生素A属于烃 | |
| B. | 维生素A不能与金属钠发生反应生成氢气 | |
| C. | 维生素A不能使酸性KMnO4溶液褪色 | |
| D. | 维生素A能发生取代、加成、酯化反应 |
15. 如表所列各组物质中,物质之间通过一步反应不能实现如图所示转化的是( )
如表所列各组物质中,物质之间通过一步反应不能实现如图所示转化的是( )
 如表所列各组物质中,物质之间通过一步反应不能实现如图所示转化的是( )
如表所列各组物质中,物质之间通过一步反应不能实现如图所示转化的是( )| a | b | c | |
| A | AlCl3 | NaAlO2 | Al(OH)3 |
| B | NaOH | Na2CO3 | NaHCO3 |
| C | Fe | FeCl3 | FeCl2 |
| D | Si | SiO2 | H2SiO3 |
| A. | A | B. | B | C. | C | D. | D |
12.某有机物的结构为 ,下列说法正确的是( )
,下列说法正确的是( )
 ,下列说法正确的是( )
,下列说法正确的是( )| A. | 1mol该有机物最多可与3mol H2发生加成反应 | |
| B. | 能使酸性KMnO4溶液褪色 | |
| C. | 1mol该有机物分别与足量的金属钠、碳酸氢钠溶液反应均产生1mol气体 | |
| D. | 与乙酸互为同系物 |
9.用稀H2SO4、NaOH和Al为原料制取Al(OH)3,有下列三种不同的途径,若制取等量的Al(OH)3则( )
甲:Al$\stackrel{H_{2}SO_{4}}{→}$Al2(SO4)2$\stackrel{NaOH}{→}$Al(OH)3
乙:Al$\stackrel{NaOH}{→}$NaAlO2$\stackrel{H_{2}SO_{4}}{→}$Al(OH)3
丙: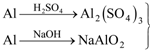 →Al(OH)3.
→Al(OH)3.
甲:Al$\stackrel{H_{2}SO_{4}}{→}$Al2(SO4)2$\stackrel{NaOH}{→}$Al(OH)3
乙:Al$\stackrel{NaOH}{→}$NaAlO2$\stackrel{H_{2}SO_{4}}{→}$Al(OH)3
丙:
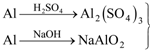 →Al(OH)3.
→Al(OH)3.| A. | 甲、乙消耗的原料同样多 | B. | 乙消耗的原料最少 | ||
| C. | 丙消耗的原料最少 | D. | 三者消耗的原料同样多 |
16.金刚石和石墨是碳元素的两种结构不同的单质(同素异形体).在100kPa时,1molC(石墨)转化为金刚石,要吸收1.895kJ的热能.据此,试判断在100kPa压强下,下列结论正确的是( )
| A. | 石墨和金刚石一样稳定 | |
| B. | 金刚石比石墨稳定 | |
| C. | 1 mol C(石墨)比1 mol C(金刚石)的总能量高 | |
| D. | 1 mol C(石墨)比1 mol C(金刚石)的总能量低 |
13.下列有机物命名正确的是( )
| A. | 2-乙基丁烷 | B. | 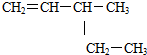 ;3-乙基-1-丁烯 ;3-乙基-1-丁烯 | ||
| C. | 2,6-二甲基-3-乙基庚烷 | D. | CH2=CH-CH=CH2;1,3,5-三己烯 |
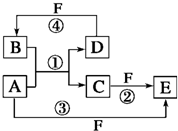 A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出)
A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出)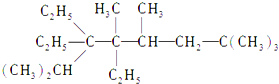 2,2,4,5,7,7-六甲基-3,3,4-乙基辛烷,
2,2,4,5,7,7-六甲基-3,3,4-乙基辛烷,