题目内容
在298K、101kPa时,已知:
2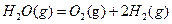 △H1
△H1
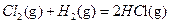 △H2
△H2
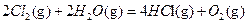 △H3
△H3
则⊿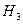 与⊿
与⊿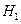 和⊿
和⊿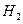 间的关系正确的是
间的关系正确的是
A .⊿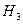 =⊿
=⊿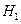 +2⊿
+2⊿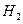 B ⊿
B ⊿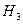 =⊿
=⊿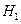 +⊿
+⊿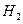
C. ⊿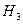 =⊿
=⊿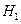 -2⊿
-2⊿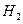 D. ⊿
D. ⊿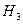 =⊿
=⊿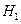 - ⊿
- ⊿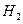
2
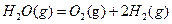 △H1
△H1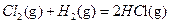 △H2
△H2 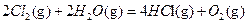 △H3
△H3则⊿
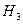 与⊿
与⊿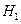 和⊿
和⊿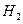 间的关系正确的是
间的关系正确的是A .⊿
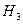 =⊿
=⊿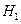 +2⊿
+2⊿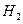 B ⊿
B ⊿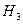 =⊿
=⊿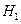 +⊿
+⊿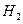
C. ⊿
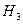 =⊿
=⊿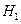 -2⊿
-2⊿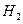 D. ⊿
D. ⊿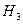 =⊿
=⊿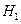 - ⊿
- ⊿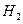
A
略

练习册系列答案
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案
相关题目
 化学键时ΔH<0[如2H(g)=H2(g) ΔH =" -" 436 kJ·mol-1]。
化学键时ΔH<0[如2H(g)=H2(g) ΔH =" -" 436 kJ·mol-1]。 
 0分)汽车尾气中含有CO、NO2
0分)汽车尾气中含有CO、NO2 等有毒气体,对汽车加装尾气净化装置,可使有毒气体相互反应转化成无毒气体。
等有毒气体,对汽车加装尾气净化装置,可使有毒气体相互反应转化成无毒气体。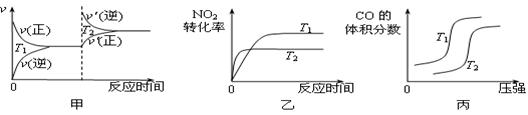 ΔH= ▲ 。对于该反应,温度不同(T2>T1)、其他条件相同时,下列图像正确的是 ▲
ΔH= ▲ 。对于该反应,温度不同(T2>T1)、其他条件相同时,下列图像正确的是 ▲  (填代号)。
(填代号)。 2O2(g)=CO2(g) +2H2O(l) △H=-890KJ/mol
2O2(g)=CO2(g) +2H2O(l) △H=-890KJ/mol 共5mol,完全燃烧生成CO2和气态水时,则放出热量(
共5mol,完全燃烧生成CO2和气态水时,则放出热量( Q)的取值范围是 ;若生成CO2和H2O的物质的量相等,则放出的热量是 。
Q)的取值范围是 ;若生成CO2和H2O的物质的量相等,则放出的热量是 。