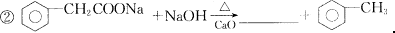题目内容
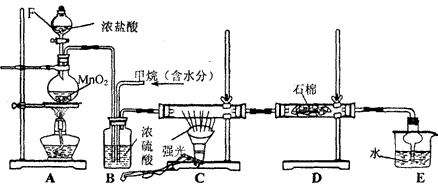
实验室制甲烷的方法是将无水醋酸钠(CH3COONa)和碱石灰混合物加强热.反应原理为:

(1)从反应所使用的药品和反应条件分析,实验室制CH4的装置应与制备________和________的装置相同.由于生成的CH4在水中溶解度很小,所以一般采用________法收集.
(2)该反应属于________反应(填反应类型).
(3)该实验中必须使用无水醋酸钠,不能使用醋酸钠晶体,否则得不到甲烷,试从反应中化学键断裂的方式分析原因:________.
(4)已知在相同的条件下使用其他的羧酸盐也可发生类似的反应,完成下列反应的化学方程式:
CH3CH2COONa+NaOH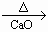 Na2CO3+________;
Na2CO3+________;
________+NaOH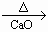 Na2CO3+
Na2CO3+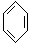 .
.
答案:
解析:
解析:
|
(1)氧气,氨气,排水集气 (2)取代 (3)因为该反应要求断裂CH3COONa和NaOH中的共价键,而二者均为离子晶体,在有水的情况下易电离,不能发生脱羧反应 (4)CH3CH3, |

练习册系列答案
 互动英语系列答案
互动英语系列答案
相关题目
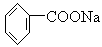
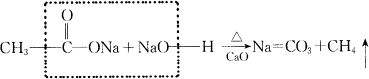
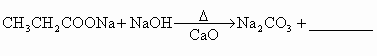 ;
;