题目内容
【题目】某校化学小组学生利用如图所列装置进行“铁与水蒸气反应”的实验,并利用产物进一步制取FeCl36H2O晶体。(图中夹持及尾气处理装置均已略去)
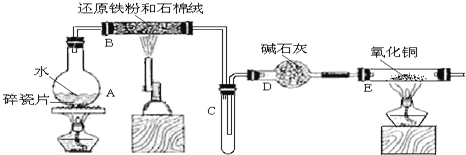
(1)装置B中发生反应的化学方程式是______。
(2)装置E中的现象是______。
(3)停止反应,待B管冷却后,取其中的固体,加入过量稀盐酸充分反应,过滤。写出可能发生的有关反应化学方程式:______。
(4)该小组学生利用上述滤液制取FeCl36H2O晶体,设计流程如图所示:
![]()
①步骤I中通入Cl2的作用是________。
②简述检验滤液中Fe3+的操作方法_______。
③步骤Ⅱ从FeCl3稀溶液中得到FeCl36H2O晶体的主要操作包括:_______。
【答案】3Fe+4H2O(g)![]() Fe3O4+4H2黑色的粉末变成紫红色,管壁产生水珠Fe3O4+8HCl=FeCl2+2FeCl3+4H2O、Fe+2HCl=FeCl2+H2↑、Fe+2FeCl3=3FeCl2将Fe2+氧化成Fe3+取少量滤液,滴入几滴KSCN溶液,观察溶液是否变红色加热浓缩、冷却结晶、过滤
Fe3O4+4H2黑色的粉末变成紫红色,管壁产生水珠Fe3O4+8HCl=FeCl2+2FeCl3+4H2O、Fe+2HCl=FeCl2+H2↑、Fe+2FeCl3=3FeCl2将Fe2+氧化成Fe3+取少量滤液,滴入几滴KSCN溶液,观察溶液是否变红色加热浓缩、冷却结晶、过滤
【解析】
A中圆度烧瓶在加热条件下可提供水蒸气,B在加热条件下,铁与水蒸气反应生成四氧化三铁和氢气,氢气经干燥,在C中用向下排空法可收集到氢气,D为干燥装置,在加热条件下氢气与氧化铜反应生成铜和水,据此解答该题。
(1)装置B中铁粉与水蒸气在高温下发生反应生成四氧化三铁和氢气,反应的化学方程式为3Fe+4H2O(g)![]() Fe3O4+4H2;
Fe3O4+4H2;
(2)装置B中铁与水蒸气反应生成的氢气,经碱石灰干燥后加入装置E,氧化铜与氢气加热发生反应生成了铜和水,所以反应的现象为:黑色的粉末变成紫红色,管壁产生水珠;
(3)在固体中加入过量稀盐酸后四氧化三铁、铁和盐酸以及铁和氯化铁之间发生反应,其方程式为Fe3O4+8HCl=FeCl2+2FeCl3+4H2O、Fe+2HCl=FeCl2+H2↑、Fe+2FeCl3=3FeCl2;
(4)①因为氯气具有强氧化性,所以能将二价铁离子氧化为三价铁离子,因此步骤I中通入Cl2的作用是将Fe2+氧化成Fe3+;
②检验三价铁应该用KSCN溶液,观察是否变红,即检验滤液中Fe3+的操作方法是:取少量滤液,滴入几滴KSCN溶液,观察溶液是否变红色;
③由FeCl3稀溶液得到FeCl36H2O晶体需加热浓缩、冷却结晶、过滤。