题目内容
【题目】关于室温下下列溶液的说法不正确的是
编号 | ① | ② | ③ | ④ |
溶液 | 氨水 | 氢氧化钠溶液 | 盐酸 | 醋酸溶液 |
pH | 11 | 11 | 3 | 3 |
A.水的电离程度:①=②=③=④
B.分别加水稀释10倍,溶液的pH:①>②>③>④
C.①、③两溶液等体积混合:c(Cl-)>c(NH)>c(H+)>c(OH-)
D.V1 L溶液②与V2 L溶液③混合,若V1∶V2=9∶11,则混合溶液pH=4(忽略溶液体积变化)
【答案】C
【解析】酸或碱抑制水电离,酸中氢离子浓度和碱中氢氧根离子浓度相等,所以它们抑制水电离程度相等,则水的电离程度①=②=③=④,故A正确;加水稀释促进弱电解质电离,导致稀释后醋酸pH小于盐酸,氨水pH大于氢氧化钠,所以它们分别稀释10倍后,溶液的pH:①>②>③>④,故B正确;①和③等体积混合,氨水过量导致溶液呈碱性,则c(H+)<c(OH-),根据电荷守恒得c(Cl-)<c(NH),故C错误;常温下,V1 L溶液②与V2 L溶液③混合,若V1∶V2=9∶11,混合溶液中c(H+)=![]() mol/L=10-4 mol/L,所以混合溶液的pH=4,故D正确。
mol/L=10-4 mol/L,所以混合溶液的pH=4,故D正确。

【题目】【2017河南模拟】某课题组设计实验探究SO2的性质.
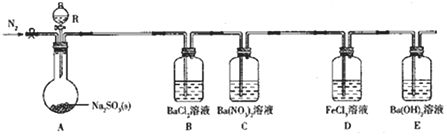
实验现象:B中无沉淀生成,C中有白色沉淀;D中溶液颜色变浅,E中产生白色沉淀.
(1)仪器R的名称是 ;
(2)实验室在常温下用80%的硫酸与亚硫酸钠粉末反应制备SO2,写出A中反应的化学方程式: ;
(3)部分实验步骤如下:连接装置、检查气密性、装药品,向装置中通入一段时间N2,然后启动A中反应.“通入一段时间的N2”的目的是 ;
(4)探究装置C中通入SO2的量与产物的关系.
①他们提出如下猜想:
猜想1:通入过量的SO2,则发生反应的离子方程式为Ba2++2NO3﹣+3SO2+2H2O═BaSO4↓+2SO42﹣+2NO+4H+.
猜想2:通入少量的SO2,则发生反应的离子方程式为 ;
②请你帮他们设计实验证明猜想1和猜想2哪个合理,完成下列实验:
提供试剂:溴水、铜粉、Ba(NO3)2溶液、BaCl2溶液、Na2CO3溶液
实验步骤 | 实验现象及结论 |
取少量C中反应后溶液于试管中, |
(5)下列可检验装置D反应后溶液中是否有Fe2+的最佳试剂是 (填字母).
a.KSCN溶液 b.NaOH溶液 c.K3[Fe(CN)6]溶液 d.KSCN溶液和双氧水
(6)常温下,实验完毕后,分离、提纯装置E中白色固体M,取适置M于试管中,滴少量盐酸(M剩余),所得溶液的pH 7(填“>”“<”或“=”)。