题目内容
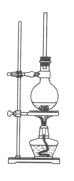
【题目】某同学用下图所示装置制取氯水并进行相关实验。

(1)装置②中反应的化学方程式是 。装置②中的NaOH溶液换成下列 也可以起到尾气处理的作用(填字母)。
a.NaCl溶液 b.FeSO4溶液 c.Na2SO3溶液
(2)实验进行一段时间后,装置①中溶液呈黄绿色,由此说明该溶液中一定含有的物质是 (填化学式)。
(3)取少量装置①中的溶液滴在蓝色石蕊试纸上,试纸先变红后褪色,说明氯水具有 性。
(4)已知将氯气通入热的氢氧化钠溶液中,可发生如下反应:Cl2 + NaOH → A + NaClO3 +H2O(未配平)其中,A的化学式是 。
【答案】(1)Cl2+2NaOH==NaCl+NaClO+H2O;bc
(2)Cl2(3)酸性、漂白性(或强氧化性)(4)NaCl
【解析】(1)氯气和氢氧化钠溶液反应生成氯化钠、次氯酸钠和水,反应方程式为:Cl2+2NaOH=NaCl+NaClO+H2O,装置②中的NaOH溶液的作用是吸收多余的氯气,防止污染空气,因此可以换成FeSO4溶液、Na2SO3溶液,通过氧化还原反应,吸收氯气,氯化钠溶液不能吸收氯气,故选bc;故答案为:Cl2+2NaOH=NaCl+NaClO+H2O;bc;
(2)只有氯气呈黄绿色,其它物质都呈无色,所以含有Cl2,故答案为:Cl2;
(3)蓝色石蕊遇酸变红色,次氯酸具有漂白性,取少量装置①中的溶液滴在蓝色石蕊试纸上,试纸先变红后褪色,说明氯水具有酸性和漂白性,故答案为:酸性、漂白性;
(4)根据氧化还原反应的特征,氯的化合价有升高也有降低,Cl2→NaClO3氯的化合价升高,而A中氯的化合价比0价低,所以A中的氯是-1价,所以A是NaCl,故答案为:NaCl。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目