题目内容
【题目】[2017天津节选]某混合物浆液含有Al(OH)3、MnO2和少量Na2CrO4。考虑到胶体的吸附作用使Na2CrO4不易完全被水浸出,某研究小组利用设计的电解分离装置(见图2),使浆液分离成固体混合物和含铬元素溶液,并回收利用。回答Ⅰ和Ⅱ中的问题。
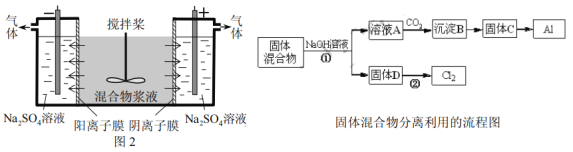
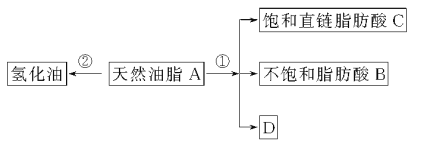
Ⅰ.固体混合物的分离和利用(流程图中的部分分离操作和反应条件未标明)
(1)反应①所加试剂NaOH的电子式为_________。B→C的反应条件为__________,C→Al的制备方法称为______________。
Ⅱ.含铬元素溶液的分离和利用
(2)用惰性电极电解时,![]() 能从浆液中分离出来的原因是__________,分离后含铬元素的粒子是_________;阴极室生成的物质为___________(写化学式)。
能从浆液中分离出来的原因是__________,分离后含铬元素的粒子是_________;阴极室生成的物质为___________(写化学式)。
【答案】(1)![]() 加热(或煅烧) 电解法
加热(或煅烧) 电解法
(2)在直流电场作用下,![]() 通过阴离子交换膜向阳极室移动,脱离浆液
通过阴离子交换膜向阳极室移动,脱离浆液
![]() 和
和![]() NaOH和H2
NaOH和H2
【解析】惰性电极电解混合物浆液时,Na+移向阴极,![]() 移向阳极。Al(OH)3、MnO2剩余在固体混合物中。固体混合物中加入NaOH溶液时,Al(OH)3转化为
移向阳极。Al(OH)3、MnO2剩余在固体混合物中。固体混合物中加入NaOH溶液时,Al(OH)3转化为![]() ,通入CO2转化为Al(OH)3沉淀,再加热分解为Al2O3,最后熔融电解得Al。
,通入CO2转化为Al(OH)3沉淀,再加热分解为Al2O3,最后熔融电解得Al。
(1)NaOH的电子式为![]() ;根据上述分析,B→C的条件为加热或煅烧,C→Al的制备方法称为电解法。
;根据上述分析,B→C的条件为加热或煅烧,C→Al的制备方法称为电解法。
(2)用惰性电极电解时,在直流电场作用下,![]() 通过阴离子交换膜向阳极室移动,脱离浆液,从而使
通过阴离子交换膜向阳极室移动,脱离浆液,从而使![]() 从浆液中分离出来;因2
从浆液中分离出来;因2![]() +2H+
+2H+![]()
![]() +H2O,所以分离后含铬元素的粒子是
+H2O,所以分离后含铬元素的粒子是![]() 和
和![]() ;阴极室H+放电生成H2,剩余的OH与透过阳离子交换膜移过来的Na+结合生成NaOH,所以阴极室生成的物质为NaOH和H2。
;阴极室H+放电生成H2,剩余的OH与透过阳离子交换膜移过来的Na+结合生成NaOH,所以阴极室生成的物质为NaOH和H2。

练习册系列答案
相关题目