题目内容
【题目】下图为江西省某城市的市区及近郊图,根据图中信息,回答下列问题。
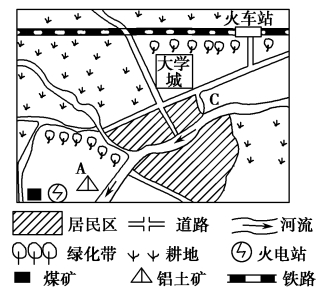
(1)图中A地区应优先发展的大型工业部门是炼铝工业,试分析该工业在此处布局的区位优势。
(2)该城市计划在C地区兴建一个新型工业园区(以电子工业为主)。简述这样规划的主要依据。
【答案】
(1)因为附近有煤矿和铝土矿,接近原料、燃料供应地;靠近河流,水源充足;靠近公路、河流,交通运输便利;处在与当地盛行风向垂直的郊外;河流的下游,对城市环境污染较小。
(2)接近大学城,科技力量较强;交通运输便利;距重工业区较远,污染小,环境条件好。
【解析】
试题分析:
(1)图示甲处有丰富的铝土资源,且靠近电站,能源丰富,故适宜发展炼铝工业。炼铝工业属于动力指向型工业,影响其区位布局的因素主要从矿产资源、能源、交通、水源和环境等方面分析。从资源条件看,甲附近有丰富的旅途矿资源,原料丰富。靠近电站,满足炼铝工业对能源的需求。从对环境的影响来看,江西省位于东部季风区,盛行西北-东南季风,甲处位于盛行风垂直的郊外,且位于河流流经城市的下游地区,对城区的污染小。从交通条件来看,靠近公路、河流,水运和陆运便利。
(2)影响电子工业布局的主导因素为科技、快速交通和环境。读图可知,C区域位于大学城附近,有丰富的科技人才。有多条干线经过,交通便利。离工业区远,受影响小,环境条件好。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目