题目内容
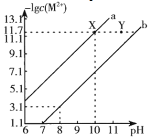
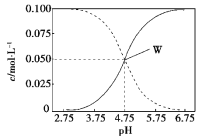
【题目】25 ℃时,有c(CH3COOH)+c(CH3COO)=0.1 mol·L1的一组醋酸、醋酸钠混合溶液,溶液中c(CH3COOH)、c(CH3COO)与pH的关系如图所示。下列有关溶液中离子浓度关系的叙述不正确的是
A.pH=5.5的溶液中:c(CH3COO—)>c(CH3COOH)>c(H+)>c(OH)
B.pH=3.5的溶液中:c(Na+)+c(H+)c(OH)+c(CH3COOH)=0.1 mol·L1
C.W点所表示的溶液中:c(Na+)+c(H+)=c(CH3COOH)+c(OH)
D.向W点所表示的1.0 L溶液中通入0.05 mol HCl气体(溶液体积变化可忽略):c(H+)=c(CH3COOH)+c(OH)
【答案】D
【解析】本题考查盐的水解,溶液中离子浓度的大小比较。分析可知图中实线是c(CH3COO),虚线是c(CH3COOH)。A.由图像可知pH=5.5的溶液中:c(CH3COO)>c(CH3COOH),溶液显酸性,则c(H+)>c(OH),且水解及电离程度较小,所以c(CH3COO)>c(CH3COOH)>c(H+)>c(OH),正确;B.pH=3.5的溶液中,c(CH3COOH)>c(CH3COO),根据电荷守恒c(Na+)+c(H+)=c(CH3COO)+c(OH),已知c(CH3COOH)+c(CH3COO)=0.1 molL1,则c(Na+)+c(H+)c(OH)+c(CH3COOH)=0.1 mol·L1,正确;C.W点表示溶液中c(CH3COOH)=c(CH3COO)=0.05 mol·L1,根据电荷守恒c(Na+)+c(H+)=c(CH3COO)+c(OH),则c(Na+)+c(H+)=c(CH3COOH)+c(OH),正确;D.向W点所表示溶液中通入0.05 molHCl气体,由电荷守恒:c(Na+)+c(H+)=c(CH3COO)+c(OH)+c(Cl),由物料守恒:c(Na+)+c(Cl)=c(CH3COO)+c(CH3COOH)=0.1 mol·L1,无法得到c(H+)=c(CH3COOH)+c(OH),错误。答案选D。