题目内容
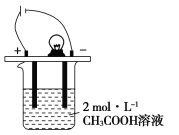
【题目】(1)氧化还原反应中实际上包含氧化和还原两个过程。下面是一个发生还原过程的反应式:![]() +4H++3e―→NO↑+2H2O。在下列四种物质KMnO4、Na2CO3、KI、Fe2(SO4)3中的一种物质(甲)中滴加少量稀硝酸能使上述还原过程发生。
+4H++3e―→NO↑+2H2O。在下列四种物质KMnO4、Na2CO3、KI、Fe2(SO4)3中的一种物质(甲)中滴加少量稀硝酸能使上述还原过程发生。
①写出并配平该氧化还原反应的化学方程式:______________________。
②上述反应中被还原的元素是________,还原剂是________。
③反应生成0.3 mol H2O,则转移电子的数目为________mol。
(2)请配平下面化学方程式。
____CH3CH2OH+____KMnO4―→____CH3CHO+____MnO2+____KOH+____H2O。
【答案】(1)①8HNO3+6KI===6KNO3+3I2+2NO↑+4H2O(3分) ②+5价N(或用文字表达) (1分) KI(1分)
③0.45(3分) (2)3 2 3 2 2 2(共2分)
【解析】(1)①题给四种物质中,能发生氧化反应的只有KI,被还原的元素为N,还原剂是KI,反应的方程式应为6KI+8HNO3===6KNO3+2NO↑+3I2+4H2O。②被还原的元素为硝酸中+5价的N,还原剂是KI。③反应6KI+8HNO3===6KNO3+2NO↑+3I2+4H2O中转移的电子数为6e,即每生成4 mol H2O,转移6 mol电子。因此若生成0.3 mol H2O,转移0.45 mol电子。
(2)根据观察法,设KMnO4的化学计量数为1,则MnO2和KOH的化学计量数均为1,根据C守恒,设CH3CH2OH和CH3CHO的化学计量数为x,根据H守恒,H2O的化学计量数为![]() (6x4x1),最后根据O守恒有:x+4=x+2+1+
(6x4x1),最后根据O守恒有:x+4=x+2+1+![]() (2x1),解得:x=
(2x1),解得:x=![]() ,平衡后得:3CH3CH2OH+2KMnO4―→3CH3CHO+2MnO2+
,平衡后得:3CH3CH2OH+2KMnO4―→3CH3CHO+2MnO2+
2KOH+2H2O。

 名校课堂系列答案
名校课堂系列答案