题目内容
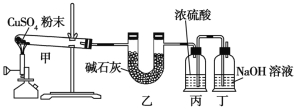
【题目】已知CuSO4![]() CuO+SO2↑+SO3↑+ O2↑。某班化学学习小组称取10.0 g CuSO4粉末,用如图所示装置进行加热至质量不再变化为止。甲、乙、丙、丁四个装置的质量变化数据如表所示。
CuO+SO2↑+SO3↑+ O2↑。某班化学学习小组称取10.0 g CuSO4粉末,用如图所示装置进行加热至质量不再变化为止。甲、乙、丙、丁四个装置的质量变化数据如表所示。
装置 | 甲(耐高温试管+CuSO4) | 乙 | 丙 | 丁 |
反应前 | 42.0 g | 75.0 g | 260.0 g | 140.0 g |
反应后 | 37.0 g | 79.5 g | 260.0 g | 140.0 g |
下列有关判断正确的是
A.装置丁的作用只是吸收S的氧化物尾气
B.生成的氧气在标准状况下的体积为350 mL
C.生成的CuO为6.0 g
D.甲中发生反应的化学方程式为6CuSO4![]() 6CuO+4SO3↑+2SO2↑+O2↑
6CuO+4SO3↑+2SO2↑+O2↑
【答案】B
【解析】装置丁中的NaOH溶液既吸收尾气,又防止大气中的酸性气体逆向进入装置乙,对实验结果造成影响,A项错误;干燥管乙中吸收的是SO2、SO3,其质量之和为 4.5 g,O2质量为42.0 g37.0 g4.5 g=0.5 g,即标准状况下的O2体积为350 mL,B项正确;CuO的质量为10.0 g4.5 g0.5 g=5.0 g,C项错误;由上述数据可推知反应物与部分生成物的物质的量之比的关系,即n(CuSO4)∶n(CuO)∶n(O2)=![]() ∶
∶![]() ∶
∶![]() =4∶4∶1,D项错误。
=4∶4∶1,D项错误。

练习册系列答案
相关题目