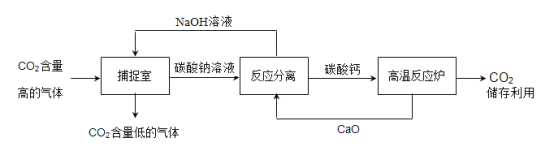
【题目】某小组在学习“二氧化碳制取的研究”课题时,进行了一系列探究实验。请你一起参与他们的活动,并回答以下问题。探究活动一:能否用排水法收集CO2
(查阅资料)(1)标况下,1体积的水溶解1体积的CO2
(2)一定浓度的稀盐酸和石灰石反应时,CO2气体生成和从水面逸出的速率远大于其溶解和与水反应的速率;
(3)向澄清的石灰水中通入过量的CO2发生了如下反应;CaCO3+H2O+CO2=Ca(HCO3)2
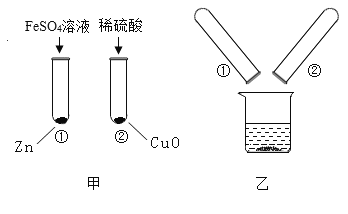
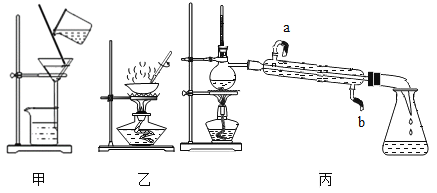
(实验探究)甲、乙两位同学分别用排水法和向上排空气法收集两瓶体积相同的CO2
甲 | 乙 | ||
实验步骤 | (1)甲、乙两位同学各收集一瓶CO2(两个集气瓶体积相同) | 向上排空气法收集并验满(理由:CO2_____,且不与空气的成分发生反应;验满方法:_____) | 排水法收集,无需验满(集满现象:_____) |
(2)向集气瓶中倒入等体积适量的澄清石灰水 | 石灰水先浑浊后变澄清所需时间较长 | 石灰水先浑浊后变澄清所需时间较短 |
(实验结论)可以用排水法收集CO2而且,与向上排空气法相比,排水法在收集CO2时有以下优点_____。
活动小组的同学还发现块状石灰石和适量稀盐酸反应至气泡逸出不明显后,测得其残留液pH=2.对此他们继续进行探究:
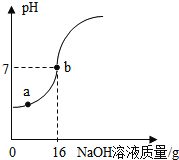
探究活动二:反应后溶液pH的变化取适量反应后的溶液。逐滴滴入碳酸钠溶液,并用pH数字探测仪连续监测,得曲线如图(纵坐标为pH,横坐标为时间);
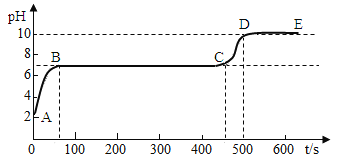
(1)请解释反应后溶液pH=2可能的原因:_____
(2)写出AB段内有关化学方程式:_____。
(3)写出BC“平台”段化学方程式:_____。
(4)CD段上升的原因是:_____。
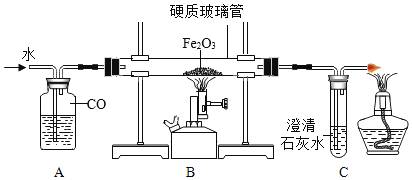
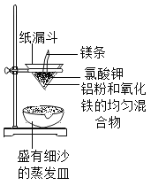
【题目】铝和氧化铁的反应:2A1+Fe2O3![]() Al2O3+2Fe,称为“铝热反应”(如图所示),引燃镁条,漏斗内的物质熔化,镁条燃尽,漏斗下端仍持续产生大量熔融物落入沙中,该熔融物可用于焊接铁轨。
Al2O3+2Fe,称为“铝热反应”(如图所示),引燃镁条,漏斗内的物质熔化,镁条燃尽,漏斗下端仍持续产生大量熔融物落入沙中,该熔融物可用于焊接铁轨。
(1)实验中镁条的作用是_____;氧化铁和铝粉都用粉末状的,原因是_____。
(2)某学习兴趣小组对所得熔融物的成分进行了探究。
(查阅资料)
①金属铝不但能和酸溶液(如稀盐酸)反应产生氢气,还能和强碱溶液(如氢氧化钠溶液)反应产生氢气。
②Al、A12O3、Fe、Fe2O3的熔点、沸点数据如下:
物质 | A1 | Al2O3 | Fe | Fe203 |
熔点/℃ | 660 | 2054 | 1535 | 1462 |
沸点/℃ | 2467 | 2980 | 2750 | - |
(实验猜想)
(3)某同学推测,铝热反应所得到的熔融物应是铁铝合金。理由是:该反应放热能使铁熔化,而铝的熔点比铁低,此时液态的铁和铝熔合形成铁铝合金。你认为他的解释是否合理?_____(填“合理”或“不合理”)。
(4)铝与稀盐酸反应的化学方程式为_____。
(5)请你根据已有知识找出一种验证产物中有Fe的最简单的方法:_____。
(实验验证)
(6)设计一个简单的实验方案,证明上述所得的熔融物中含有金属铝,请填写下列表格:
实验步骤 | 实验现象 | 实验结论 |
取少量冷却后的熔融物于试管中,加入_____ | _____ | 熔融物中含有铝 |