【题目】同学们对市场上烧烤花蛤用的“锡纸”产生了浓厚兴趣。查阅资料获知:市售锡纸也称作铝箔、铝箔锡纸等。那么“锡纸”中的金属是什么呢?
![]()
(猜想与假设)同学们结合金属的颜色、活动性、价格等因素。猜想:可能是锡、铝、镁、铁、中的一种。
(查阅资料)金属锌似晶体状,室温下,锌较硬且相当脆;氧化铝的熔点2054℃;
(初步探究)同学们结合金属的主要的物理和化学特性设计了如下实验:
序号 | 实验方案 | 现象 | 结论 |
1 | _____ | 无明显现象 | 金属不可能是铁 |
2 | 用坩埚钳夹取打磨后的“锡纸”条,放在酒精灯上点燃。 | “锡纸”条熔化但没有滴落,也没燃烧。 | 金属不可能是_____ |
(深入探究)同学们对于“锡纸”到底是什么金属,进行了深入的实验探究。
(1)第一组同学将“锡纸”条卷成和铁钉一样粗细,先在20%的盐酸中浸泡至产生较多气泡,再取蒸馏水清洗,然后浸在蒸馏水中备用。浸泡在盐酸中目的是_____。
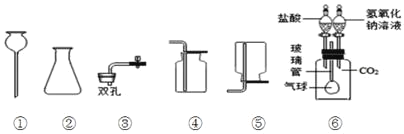
(2)将打磨后的铁钉和备用的“锡纸”条分别放入到装有5mL 15% 的稀盐酸中(如图所示)。观察到“锡纸”条表面产生的气泡速率比铁钉快。
(实验结论)制作“锡纸”的金属是_____。写出“锡纸”条与稀盐酸反应的化学方程式:_____。
(交流与反思)
(3)“锡纸”在酒精灯上加热,“锡纸”熔化但没有滴落的原因是:_____。
(4)第二组同学,将备用的“锡纸”条放入到装有硫酸锌溶液的试管中。一段时间后,未观察到明显现象。同学们讨论分析可能的原因是:①反应速率较慢,生成物太少;②_____。
(5)同学们在老师的帮助下,将3克烘干的备用“锡纸”片放入装有硫酸锌溶液的试管中,5分钟后,取出“锡纸”片,洗涤、烘干、称量。反应后金属质量范围是_____。
【题目】小华同学无意将NaOH溶液与NaHCO3溶液混合,发现无明显现象。对此他产生疑问:两种物质是否发生了化学反应?在老师的帮助下,他进行了以下探究。

(查阅资料)NaHCO3溶液能与NaOH溶液反应生成一种新盐和一种常见的液体氧化物。
NaHCO3在50℃开始分解。
(实验探究)用一定溶质的质量分数的NaHCO3、NaOH和Na2CO3三种溶液进行如下实验,为设计实验方案提供参考。
NaHCO3溶液 | NaOH溶液 | Na2CO3溶液 | |
加入稀盐酸 | 现象Ⅰ | 无明显变化 | 产生气泡 |
加入澄清石灰水 | 溶液变浑浊 | 无明显变化 | 现象Ⅱ |
加入CaCl2稀溶液 | 无明显变化 | 溶液变浑浊 | 溶液变浑浊 |
加热溶液至沸腾,将 气体通入澄清石灰水 | 澄清石灰水 变浑浊 | 澄清石灰水 无明显变化 | 澄清石灰水 无明显变化 |
(1)表中的现象Ⅰ为_____,发生现象Ⅱ对应反应的化学方程式为_____。
实验过程
(实验探究)证明反应生成了新盐
(2)NaHCO3溶液能与NaOH溶液反应生成新的盐是_____(填物质名称)。同学们选用上表实验中的药品,设计了如图所示实验,先在NaHCO3 溶液中加入A溶液,无明显现象,再滴加NaOH溶液,溶液变浑浊,则A溶液是_____。
(3)有同学提出上述实验方案有问题,其理由是_____。为了达到实验目的,你需要继续进行的操作是_____。
(交流反思)证明反应后NaHCO3不存在
(4)同学们参考上表中的实验,又设计了一个实验,虽然没有观察到明显的实验现象,但可以证明反应发生了,你的实验方案是_____。