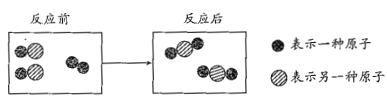
【题目】空气中氧气含量测定的再认识。
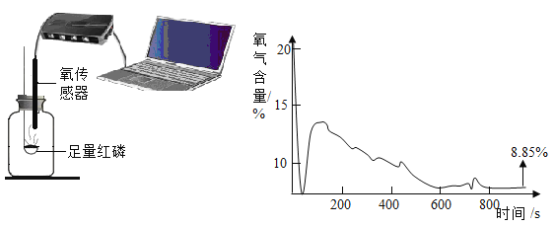
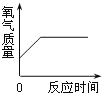
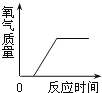
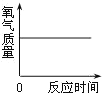
(一)某化学实验小组点燃红磷,并用氧传感器测定空气中的氧气含量并采集数据如上图。
(1)红磷在瓶中燃烧产生的现象是_____,红磷燃烧的化学方程式是_____。
(2)开始时氧气的含量持续下降,一方面是氧气被消耗,另一方面是生成物大量和氧传感器接触,但在110s时氧气的含量又有所上升,其可能原因是_____。
(3)从以上数据分析最终集气瓶中的氧气是否完全消耗_____。
(二)针对以上实验测定结果实验小组同学对该实验做了以下两种改进:

Ⅰ.根据铁在空气中生锈的原理设计如图实验装置,测定空气中氧气含量。
查资料:装置中饱和食盐水、活性炭会加速铁生锈。
测得实验数据如下表:
测量项目 | 实 验 前 | 实 验 后(冷却到室温后) | ||
烧杯中水的体积 | 烧杯中剩余水的体积 | 集气瓶(扣除内容物)的容积 | 导管的容积 | |
体积/mL | 80.0 | 54.5 | 126.0 | 6.0 |
(1)铁生锈过程发生复杂的化学反应,首先是铁与氧气、水反应生成氢氧化亚铁[Fe(OH)2],写出该反应的化学方程式_____;该反应的基本类型是_____。
(2)根据上表数据计算,改进实验后测得的空气中氧气的体积分数是_____%(结果精确到0.1%)。
(3)从实验原理角度分析,改进后的实验结果比前者准确度更髙的原因是:
①_____;②_____。
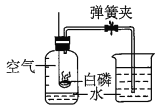
Ⅱ.将足量白磷放在集气瓶中,白磷能发生缓慢氧化从而消耗氧气,并用压强传感器测定瓶中压强的变化,根据压强的变化来计算空气中氧气的含量,实验装置及数据采集如下图。
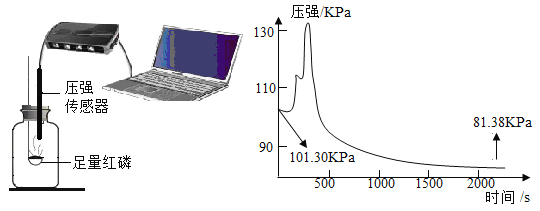
(1)在开始200s压强增大,增大的原因是_____。
(2)用上图所示数据计算用这种方法测得的空气中氧气的体积分数是_____%(结果精确到0.1%)。
(三)结论:测定空气中氧气含量用燃烧法测定结果误差较大,用缓慢氧化误差较小。