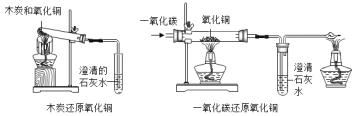
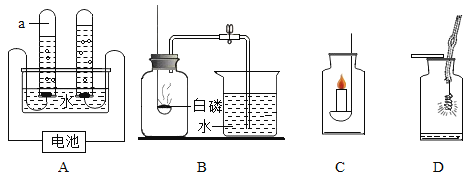
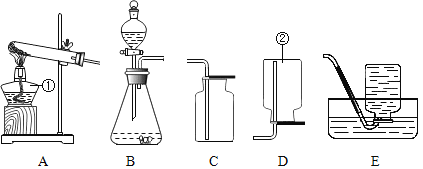
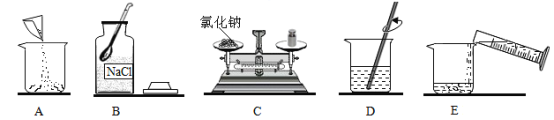
【题目】某研究小组对自动充气气球(如图1)进行下列探究。

【查阅资料】
①该气球的充气原理是:通过挤破液体包,使液体与白色粉末接触产生二氧化碳气体,实现气球自动充气。
②氯化钙水溶液呈中性,碳酸钠、碳酸氢钠的水溶液均呈碱性。
③用一定溶质质量分数的NaHCO3和Na2CO3溶液进行实验,实验现象记录如下:
NaHCO3溶液 | Na2CO3溶液 | |
加入澄清石灰水 | 溶液变浑浊 | 溶液变浑浊 |
加入CaCl2溶液 | 无明显变化 | 溶液变浑浊 |
加热溶液至沸腾,将 气体通入澄清石灰水 | 澄清石灰水 变浑浊 | 澄清石灰水 无明显变化 |
探究1:液体包内溶液的酸碱性
室温时,用pH试纸测得溶液的pH=3,则该溶液呈________性。
探究2:白色粉末的成分
【猜想与假设】甲同学认为是碳酸钙;乙同学认为是碳酸钠;丙同学认为是碳酸氢钠;丁同学认为是碳酸钠和碳酸氢钠的混合物。
【进行实验】
(1)将少量白色粉末放入水中搅拌,观察到____________,说明甲同学的猜想不正确。
(2)室温时,分别向盛有碳酸氢钠、碳酸钠和白色粉末样品的锥形瓶中注入等体积、足量的10%的盐酸(装置如图2),记录如下表:

实验编号 | 锥形瓶内物质 | 最终得到CO2体积/mL | |
名称 | 质量/g | ||
Ⅰ | 碳酸氢钠 | 0.10 | V1 |
Ⅱ | 碳酸钠 | 0.10 | V2 |
Ⅲ | 白色粉末 | a | V1 |
【解释与结论】
(1)实验Ⅰ的化学方程式为_________________________。
(2)表中a=________;V1______V2(填“>”、“<”或“=”)。
(3)上述实验得出的结论及判断依据是___________________________。
【反思与评价】
老师指出还可以采用更简单的方法得出与上述实验(2)相同的结论,实验方案为_________。
【题目】NH4Cl和Na2SO4的溶解度表及溶解度曲线如下。下列说法正确的是 ( )
温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度S/g | NH4Cl | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 60.2 |
Na2SO4 | 9.6 | 20.2 | 40.8 | 48.4 | 47.5 | 47.0 | |
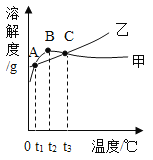
A.甲为NH4Cl
B.t2℃应介于30℃~50℃
C.甲、乙饱和溶液从t3℃降温到t2℃,溶质的质量分数都变小
D.等质量的甲、乙饱和溶液从t1℃升温到t3℃,为使其溶液恰好饱和,加入的甲、乙固体质量相等
【题目】实验是科学探究的重要方法.如图是测定空气中氧气含量实验的两套装置图,请结合图示回答有关问题。
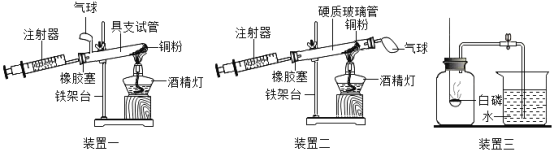
(1)利用装置二进行实验,根据下表提供的实验数据,完成下表.
硬质玻璃管中空气的体积 | 反应前注射器中空气体积 | 反应后注射器中气体体积 | 实验测得空气中氧气的体积分数 |
55ml | 25ml | 13ml | ____ |
出现上述实验结果,可能的原因______.
(2)装置一、二与装置三对比,其优点是_____.理由是_______