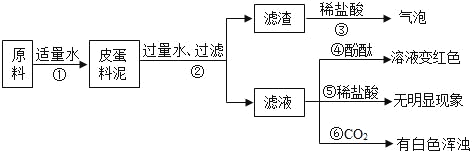
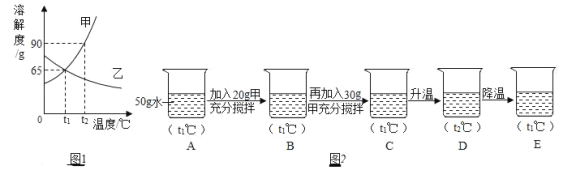
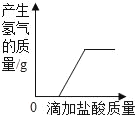
【题目】实验室中有一瓶标签受损的无色溶液,如图1所示,老师提示这是一瓶初中常用的溶液,要求同学们确认其溶质成分。
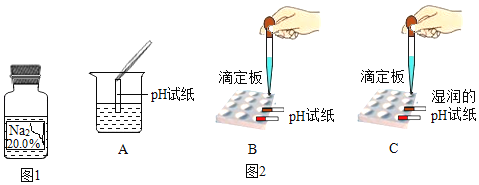
【提出猜想】①氯化钠②氢氧化钠③硫酸钠④碳酸钠
【查阅资料】氯化钠和硫酸钠溶液pH=7可溶性硫酸盐遇到可溶性的钡盐会产生白色沉淀。
【讨论分析】经过讨论,同学们一致认为猜想_____(填序号)不成立,其原因是_____。
【实验探究】为了进一步确认其成分,同学们继续进行探究:
实验步骤 | 实验现象 | 实验结论 |
(1)取该溶液少许于试管中,向其中滴加稀盐酸 | 无明显现象 | 猜想_____不成立 |
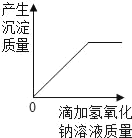
(2)取该溶液少许于试管中,向其中滴加氯化钡溶液 | _____________ | 猜想③成立 |
假如猜想④成立,写出(1)中发生的反应方程式_____。
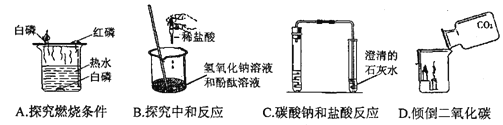
【反思与交流】有同学提出用测pH的方法也可以确定该无色溶液,如图2所示是几位同学的实验过程,其中正确的是_____。
【题目】小亮在做“盐酸中和氢氧化钠溶液”的实验时,滴加盐酸前忘了加入指示剂,导致无法判断该中和反应进行的程度。于是他对所得溶液的酸碱性进行探究。
(实验探究)稀盐酸与氢氧化钠反应的化学方程式为_____。
(提出猜想)所得溶液可能呈碱性,也可能呈_____性,还可能呈_____性。
(实验验证)
实验操作 | 实验现象 | 结论 |
用试管取该溶液1﹣2mL,滴入 1﹣2滴无色酚酞试液,振荡 | 无色酚酞试液变_____ | 溶液呈碱性 |
无色酚酞试液不变色 | 溶液呈_____ |
若无色酚酞试液不变色,为了进一步确定溶液的酸碱性,小亮提出了以下方案:
取样,加入金属锌,若有所泡产生,则所取溶液呈酸性,该反应的化学方程式为_____;若无明显现象,则溶液呈_____性。
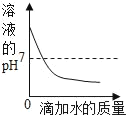
(分析论证)如图是小亮同学根据实验绘制的溶液的pH随加入溶液的质量变化的曲线。
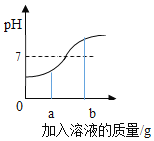
①氢氧化钠与盐酸恰好完完全反应时,溶液的pH_____7(填“>“<”或“=”)
②根据曲线判断,小亮是将_____(填“氢氧化钠溶液”或“盐酸”,下同)滴入_____中。
③当滴入溶液的质量为bg时,向所得溶液中滴加酚酞溶液,溶液颜色为_____色,此时溶液中的溶质是_____、_____。