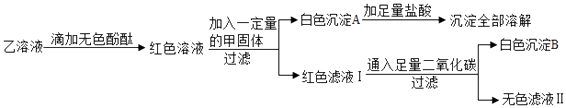
【题目】某研究小组欲检验草酸晶体样品分解产物,查阅资料知道,草酸晶体(H2C2O42H2O)在加热的条件下发生下列反应:
H2C2O42H2O ![]() 3H2O+CO↑+CO2↑
3H2O+CO↑+CO2↑
草酸晶体的其他性质如下:
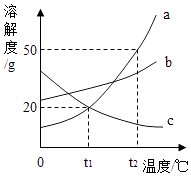
熔点 | 沸点 | 溶解度(0℃) | 热稳定性 | 与碱反应 |
101℃~102℃ | 150℃~160℃ | 3.54g | 100.1℃失去结晶水,175℃分解成CO2 , CO,H2O | 与Ca(OH)2反应产生白色沉淀(CaC2O4) |
该小组设计的装置如下:图1是加热分解装置,图2是验证分解产物的装置.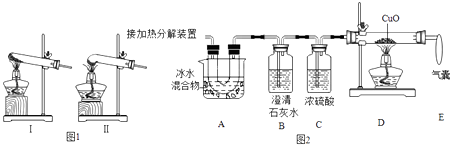
该小组称量纯碱草酸晶体的质量为10.0g,完全反应后A装置增加的质量为ag,B装置增加的质量为bg,D装置减少的质量为dg.实验过程中还能够观察到A中有液体和晶体.
(1)加热分解草酸晶体最适宜的装置是(填图1字母序号).
(2)实验过程中A装置的U型管中有晶体产生的原因是 .
(3)证明二氧化碳存在的现象是 , 气囊的作用是 .
(4)若图1中相应的加热装置中无固体剩余且不考虑装置中残留气体质量,根据A、B、C装置的质量变化能否计算分解的草酸晶体的质量?(填“能”或“不能”).
(5)若以D装置的质量变化计算分解的草酸晶体的质量,其结果比实际值(偏大、偏小或无变化)
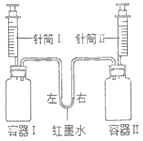
【题目】如图装置中容器Ⅰ、Ⅱ,针筒Ⅰ、Ⅱ完全相同,针筒Ⅰ、Ⅱ中装的是足量液体药品,当将针筒中液体全部加入到溶液Ⅰ、Ⅱ后,始终不能够明显观察到红墨水左高右低的是( )
容器Ⅰ药品 | 针筒Ⅰ药品 | 容器Ⅱ药品 | 针筒Ⅱ药品 | |
A | 洁净铁粉 | 水 | 洁净铁粉 | 植物油 |
B | 二氧化碳 | 氢氧化钠溶液 | 二氧化碳 | 水 |
C | 硝酸铵 | 水 | 氧化钙 | 水 |
D | 镁条 | 稀盐酸 | 氧化铜 | 稀盐酸 |
A.A
B.B
C.C
D.D