人体内一些液体的正常pH范围如下:
液体 | 胃液 | 唾液 | 胆汁 | 胰液 |
pH | 0.9﹣1.5 | 6.6﹣7.1 | 7.1﹣7.3 | 7.5﹣8.0 |
下列说法中不正确的是( )
A.胆汁和胰液显碱性
B.胃液比唾液酸性弱
C.胰液比胆汁碱性强
D.服用含氢氧化铝[Al(OH)3]的药物可以治疗胃酸过多症
下列除去杂质的方法中正确的是( )
选项 | 物质 | 杂质 | 除杂质的方法 |
A | KCl | MnO2 | 加适量水溶解、过滤、蒸发 |
B | CO2 | CO | 将气体通入足量氢氧化钠溶液 |
C | 银粉 | 锌粉 | 加入过量硫酸亚铁溶液,过滤 |
D | NaCl溶液 | Na2CO3 | 加适量硝酸钙溶液,过滤 |
A. A B. B C. C D. D
某兴趣小组在准备化学实验基本技能考查时,对以下问题进行了探究:
Ⅰ.探究酸和碱能否发生反应
方案l:甲同学向盛有少量NaOH溶液的试管中滴几滴无色酚酞试液,振荡,继续加入稀硫酸,观察到溶液由____色变成无色。甲同学得出结论:酸和碱能发生反应。
方案2:乙同学取少量NaOH溶液,测得溶液pH为10,向该溶液中加入一定量稀硫酸后,测得溶液pH为9,乙同学发现溶液pH减小了,得出结论:酸和碱能发生反应。
(交流讨论)大家同意甲同学的结论,对乙同学的实验过程提出质疑,溶液pH减小的原因还可能是稀硫酸中的水稀释了NaOH溶液;大家认为,乙同学向NaOH溶液中加入稀硫酸后,测得溶液的pH必须___7(填“等于”、“小于”、“小于或等于”)才能证明酸和碱能发生反应。请写出稀硫酸和氢氧化钠溶液反应的化学方程式___。
Ⅱ.探究酸和碱反应后溶液中溶质的成分
丙同学对探究Ⅰ中甲同学实验后的无色溶液展开探究:
(提出问题)试管中无色溶液的溶质除了酚酞还有什么?
(提出猜想)猜想一:Na2SO4;猜想二:Na2SO4、NaOH; 猜想三:___。
(交流讨论)你认为猜想__一定不正确,理由是:__。
(设计实验)
实验操作 | 实验现象 | 实验结论 | |
方案1 | 向试管中加入少量锌粒,然后加入甲同学实验后的无色溶液 | 锌粒逐渐减少,有____产生。 | 猜想三成立 |
方案 2 | 向试管中加入少量甲同学实验后的无色溶液,然后慢慢滴加NaOH溶液,并不断振荡试管 | 开始无明显现象,过一会发现_____。 |
(实验反思)为了验证猜想三成立,你认为还可选择的药品是__(填字母序号)
A BaCl2溶液 B Cu C Fe2O3
某化学兴趣小组为测定大理石中碳酸钙的含量,进行如图 1 所示实验:将过量的稀盐酸加入到20 g大理石中(其他成分不与盐酸反应),把产生的CO2气体用足量的烧碱溶液吸收,同时测量 C 瓶烧碱溶液增加的质量,结果如下表所示:
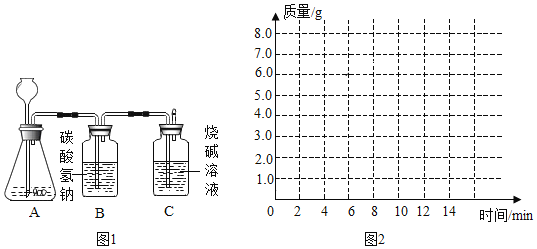
时间/分 | 0 | 2 | 4 | 6 | 8 | 10 | 12 |
C 增加质量/g | 0 | 3.0 | 5.0 | 6.0 | 6.6 | x | 6.6 |
(1)上表中,第 10 分钟时,x=__________。
(2)计算大理石样品中碳酸钙的质量分数。_________(要写计算过程)
(3)请在如图 2 的坐标纸上,以时间为横坐标,以产生 CO2 气体的质量为纵坐标,画出能够表明产生气体的质量随时间变化规律的关系曲线(假设第 8 分钟是恰好反应结束)______________。
(4)B 中所装药品为碳酸氢钠溶液,作用是吸收挥发出的 HCl 气体,该装置使测量结果________(填“偏 大”“偏小”或“没有影响”)。