��Ŀ����
����Ŀ��ij��ѧ��ȤС�����NaOH��Һ�������Ƿ�ǡ����ȫ��Ӧ������̽��������������ǵ�̽��������ش��й����⡣
��ʵ��̽����
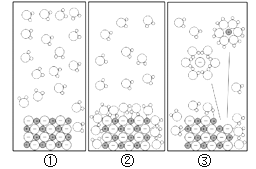
��1������һ����ͬѧ����ͼ��ʾ�ķ��������Թ��м���Լ2mLNaOH��Һ���ٵ��뼸�η�̪��Һ����Һ��졣Ȼ����������ϡ���ᣬ�ߵα���ֱ����Һǡ�ñ�Ϊ_____ɫ��֤��NaOH��Һ��ϡ����ǡ����ȫ��Ӧ��
![]()
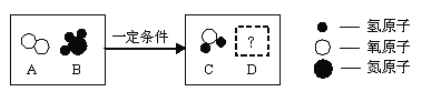
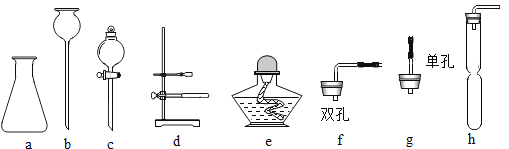
����ָ����ͼ�����еĴ���_____��
��д��NaOH��Һ��ϡ���ᷴӦ�Ļ�ѧ����ʽ_____��
��2������������ͬѧ��������ķ�������ʵ��֤����������������ǡ����ȫ��Ӧ��
ʵ�鲽�� | ʵ������ | ���� |
ȡ2mLNaOH��Һ���Թ��У�����һ������ϡ���ᣬ�ٵμ���ɫ��̪��Һ������� | û���������� | ����ǡ����ȫ��Ӧ����Һ������ |
��ʵ�鷴˼��
������һ�ڵ���ϡ����Ĺ����У����۲쵽�����������ݳ��֣�������������ݵ�ԭ�������_____��д����ѧ����ʽ����
����ͬѧ�������������֤��NaOH��Һ��ϡ����ǡ����ȫ��Ӧ����ԭ����_____��Ϊ�ˣ�����Ҫѡ��_____����һ���Լ������ٽ���ʵ�鼴�ɡ�
��3��ij��ѧ��ȤС��Ϊ�˲ⶨij������ˮ������ĺ�����ȡ100g��ˮ���ձ��У�����80g��������Ϊ10��������������Һ��ǡ����ȫ��Ӧ(��ˮ������������ɷֲ����뷴Ӧ)������㣺��ˮ�����������������_____
���𰸡��� �ѽ�ͷ�ι������Թ��� ![]()
![]() ������������Ʒ�Ӧ�����������Ҳ�۲첻������ ��ɫʯ����Һ 9.8%
������������Ʒ�Ӧ�����������Ҳ�۲첻������ ��ɫʯ����Һ 9.8%
��������
���������ƺ�ϡ����ǡ����ȫ��Ӧʱ����Һ�����ԣ���̪��Һ����ɫ�����������ƹ���ʱ����Һ�Լ��ԣ���̪��Һ���ɫ����ϡ�������ʱ����Һ�����ԣ���ɫ��̪��Һ����ɫ��
��1������һ����ͬѧ�����Թ��м���Լ2mLNaOH��Һ���ٵ��뼸�η�̪��Һ����Һ��졣Ȼ����������ϡ���ᣬ�ߵα���ϡ������������Ʒ�Ӧ��ֱ����Һǡ�ñ�Ϊ��ɫʱ��˵����Ӧ��ȫ��
�ٽ�ͷ�ιܲ��������Թ��У�ͼ�ϲ����еĴ����ǰѽ�ͷ�ι������Թ��С�
��NaOH��Һ��ϡ���ᷴӦ�����Ȼ��ƺ�ˮ����ѧ����ʽΪ![]() ��
��
[ʵ�鷴˼]
������һ�ڵ���ϡ����Ĺ����У����۲쵽�����������ݳ��֣��������ݵ�ԭ��������������ƺͿ����еĶ�����̼��Ӧ����̼���ƣ�̼���ƺ�ϡ���ᷴӦ���ɶ�����̼����ѧ����ʽΪ![]() ��
��
����ͬѧ�������������֤��NaOH��Һ��ϡ����ǡ����ȫ��Ӧ����ԭ����������������Ʒ�Ӧ�������������Һ�����ԣ���̪��Һ����ɫ��Ҳ�۲첻��������Ҫѡ����ɫʯ����Һ�������ᡣ
��3������뷴Ӧ�����������Ϊx
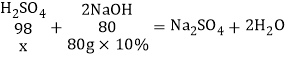
![]()
x=9.8g
��ˮ���������������Ϊ![]()

 Сѧ��ʱ��ҵȫͨ����ϵ�д�
Сѧ��ʱ��ҵȫͨ����ϵ�д� �����ÿ�ʱѵ��ϵ�д�
�����ÿ�ʱѵ��ϵ�д� ��Ԫȫ��������ϵ�д�
��Ԫȫ��������ϵ�д� �»ƸԱ����ܾ�ϵ�д�
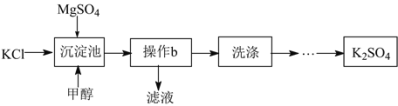
�»ƸԱ����ܾ�ϵ�д�����Ŀ��������þ���Ȼ���Ϊԭ���Ʊ�K2SO4���������¡�
��֪��20������ʵ��ܽ�������
���� | MgSO4 | MgCl2 | K2SO4 | KCl |
�ܽ��/g | 33.7 | 54.6 | 11.1 | 34.2 |
��1����������������ʵ��ܽ�������ʾ��д���������з����ĸ��ֽⷴӦ�Ļ�ѧ����ʽ_____����Ӧ���ڳ����·�����ԭ����_____��
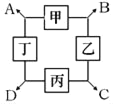
��2���������м���״���Ŀ����_____��
��3������b��������_____�����в���b��Ҫ�IJ����������ձ���_____��_____��
��4����������Ƿ�ϴ����ȫ���Լ���_____��������ţ�
a����������Һ b�Ȼ�����Һ cϡ����
����Ŀ�������NaCl��KNO3�ڲ�ͬ�¶�ʱ���ܽ�ȣ���仯������ͼ��ʾ�����������������ǣ�������
�¶�/�� | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
�ܽ��/g | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | |
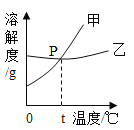
A. 100gˮ��������ܽ�KNO331.6g
B. ��ʾNaCl���ܽ�������Ǽ�
C. �¶�t�ķ�Χ������20����30��֮��
D. ��������Һ��Ϊ������Һ�����ʵ�������������