��Ŀ����
����Ŀ���Ķ����пƼ����ģ��ش����⡣
�Ͼ�������Ʒ������̥�Ⱥ�̼������α��Ϊ�������ڶ��ѧ�Һ���ʦŬ����Ŀ�ꡣ
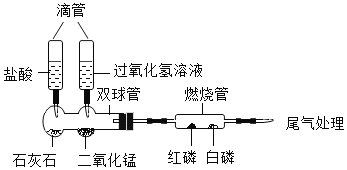
�о���Ա������һ���ó��ٽ�ˮ������̼������¼��������ٽ�ˮ�ǽ�ˮ���ȵ�����374�沢��ѹ������219������ѹ��ʹˮ��������Һ����ڵ�״̬��
�ڳ��ٽ�ˮ�Ļ����У���̼�����е��л���ת��Ϊ����������Ͷ�����̼�����壻�����ﱣ���ڲ������У����ȥ�������ڸù����в�ʹ���������¶���Խϵͣ���˲����γ��к����塣
��1�������漰�����л��ϳɲ�����_________����1�ּ��ɣ���
��2������˵����ȷ����_________������ĸ��ţ���
A ���ٽ�ˮ��Һ̬ˮ������ͬ�������ͻ�ѧ����
B ����̬ˮ���»��ѹһ��ʹˮ���Ӽ�����С
C ���ٽ�ˮ����Һ̬ˮ����̬ˮ��ɵĻ����
D �ó��ٽ�ˮ������̼����ķ����ȷ��շ�������
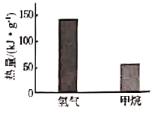
��3�������ͼ��鶼�������Դ��д��������ȫȼ��ʱ��Ӧ�Ļ�ѧ����ʽ_________�����ȼ��1 g����������ͷŵ���������ͼ��ʾ���������ȣ�������Ϊȼ�ϵ��ŵ���_________�����ճ�������ʹ�õ�ȼ�ϣ���������Լ���Ϊ��Ҫ�ɷֵ���Ȼ����ԭ����_________��д��1 �㼴�ɣ���
���𰸡����ϣ����� D CH4+2O2![]() CO2+2H2O ȼ��ʱ�ų����������� �����������ѣ�����ȡ�ɱ��ߣ�
CO2+2H2O ȼ��ʱ�ų����������� �����������ѣ�����ȡ�ɱ��ߣ�
��������
��1��������Ʒ�������л��ϳɲ��ϣ�
��2��A�����ٽ�ˮ�ǽ�ˮ���ȵ�����374�沢��ѹ������219������ѹ��ʹˮ��������Һ����ڵ�״̬�������������ʲ��ܴ�ѡ��˵������
B�����ٽ�ˮ�ǽ�ˮ���ȵ�����374�沢��ѹ������219������ѹ��ʹˮ��������Һ����ڵ�״̬��ˮ���Ӽ������ܱ��ѡ��˵������
C�����ٽ�ˮ����Һ̬ˮ����̬ˮ��ɵĴ������ѡ��˵������
D���ڳ��ٽ�ˮ�Ļ����У���̼�����е��л���ת��Ϊ����������Ͷ�����̼�����壬�ó��ٽ�ˮ������̼����ķ����ȷ��շ�����������ѡ��˵����ȷ��
��3��������ȫȼ�����ɶ�����̼��ˮ����Ӧ�Ļ�ѧ����ʽCH4+2O2![]() CO2+2H2O����ͼ��֪���������ȣ�������Ϊȼ�ϵ��ŵ���ȼ��ʱ�ų����������ࣻĿǰ�������������л�û�д���Ӧ������Դ��û�ҵ����ʡ����۵����ⷽ������������ȫ�Ĵ�������䷽����
CO2+2H2O����ͼ��֪���������ȣ�������Ϊȼ�ϵ��ŵ���ȼ��ʱ�ų����������ࣻĿǰ�������������л�û�д���Ӧ������Դ��û�ҵ����ʡ����۵����ⷽ������������ȫ�Ĵ�������䷽����

����Ŀ�����������ǿ�ѧ�о��е��ش���⡣ijУѧϰС�������ĸ�ʴΪ��Ŀ���������о���
����ʶ���ĸ�ʴ��
��1�����л����е�����Ʒ�������������_______������ĸ��ţ���
A δ���ɵ����� B ����������� C ʢˮ�IJ����ˮ��
��2���������Ҫ�ɷ���Fe2O3��xH2O��������Ԫ�صĻ��ϼ���____��
��̽�����ĸ�ʴ��
��3����С������ͼ��װ�ý���ʵ�飬��ʼʱ��Ͳ��ˮ�洦��50 mL�̶ȴ���֮��ˮ�滺�������������ˮ�����մ���Լ____������40������10����mL�̶ȴ���ԭ����____��
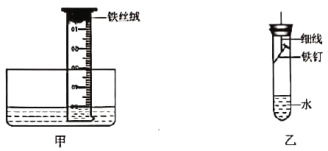
����չ̽����
��4��Сǿͬѧ��������ʵ�飺ȡ������ɰֽ��ĥ����������������ͼ�Ұ�װװ�ã�����3�죬��ȡ�������������ڲ�ͬ�¶����ظ�����ʵ�飬�õ�������������������±���
�¶�/�� | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
������������/g | 0.02 | 0.04 | 0.08 | 0.16 | 0.18 | 0.18 | 0.18 |
Сǿͬѧ��ʵ����̽��____���ض�������ʴ������Ӱ�죬������____��
��5����ͬѧ��ΪСǿ��ʵ��δ����ʵ��ӳ50���Ժ�������ʴ�Ŀ�����������50���Ժ���������û�б仯���������������û�б仯��ԭ��____���Ľ�ʵ�鷽��֤�����____��
����Ŀ��Ϊ�ⶨпͭ�Ͻ���п�ĺ�����ȡ�úϽ������ͼ 14 ʢ��ϡ�������ƿ�У�������Ӧ�� Zn+H2SO4=ZnSO4+H2�� �����ʵ���ȡƽ��ֵ�����������±���

��Ӧǰ | ��ַ�Ӧ��װ�ü���Ӧʣ���������� | |
װ�ú�������ϡ�������� | пͭ�Ͻ����� | |
342.10g | 16.00g | 357.70g |
�������Ǹ�������տ����е�ˮ���������㣺
��1�����������غ㶨��������������������
��2���úϽ���п������������