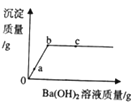题目内容
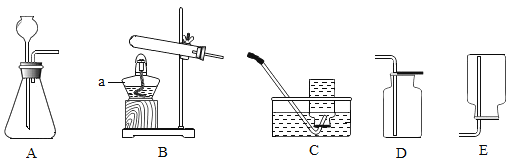
【题目】下列物质提纯所用的实验不正确的是
选项 | 物质(括号内为杂质) | 实验方法 |
A | CuO(Cu) | 在氧气流中充分加热 |
B | Fe(Al2O3) | 加入足量稀硫酸,充分反应后结晶 |
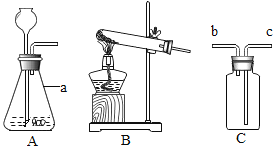
C | H2(HCl) | 通过装有NaOH 溶液的洗气瓶 |
D | KNO3 溶液(K2SO4) | 加入适量的 Ba(NO3)2 溶液,过滤 |
A.AB.BC.CD.D
【答案】B
【解析】
A、铜可与氧气在加热的条件下反应生成氧化铜,从而除去杂质铜,不符合题意;
B、加入足量稀硫酸,铁与稀硫酸反应生成硫酸亚铁和氢气,三氧化二铝和稀硫酸反应生成硫酸铝和水,充分反应后,结晶,不但除去了杂质,也除去了原物质,符合题意;
C、将混合气体通过装有NaOH 溶液的洗气瓶,![]() ,从而除去杂质,不符合题意;
,从而除去杂质,不符合题意;
D、加入适量的 Ba(NO3)2 溶液,![]() ,过滤,可除去杂质,不符合题意。
,过滤,可除去杂质,不符合题意。
故选B。

 阅读快车系列答案
阅读快车系列答案【题目】某研究小组在学习氧气的化学性质时发现:铁丝在氧气中燃烧没有火焰,而蜡烛在氧气中燃烧却有明亮的火焰。该小组同学进行了如下探究。
(1)写出铁丝在氧气中燃烧的符号表达式:_____。
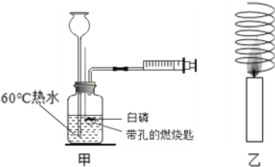
(2)探究一:蜡烛燃烧产生火焰的原因是什么?
点燃蜡烛,将金属导管一端伸入内焰,导出其中物质,在另一端管口点燃,也有火焰产生。由此可知:蜡烛燃烧产生的火焰是由_____(填“固态”或“气态”)物质燃烧形成的。
(3)探究二:物质燃烧产生火焰的根本原因是什么?
物质 | 熔点╱℃ | 沸点╱℃ | 燃烧时温度╱℃ |
石蜡 | 50∽70 | 300∽550 | 约600 |
铁 | 1535 | 2750 | 约1800 |
钠 | 97.8 | 883 | 约1400 |
由上表可知:物质燃烧能否产生火焰与其_____(填“熔点”或“沸点”)和燃烧时温度有关。通过上表中石蜡、铁的数据对比,你认为物质燃烧时,什么情况下能产生火焰_____。由此推测:钠在燃烧时,_____(填“有”或“没有”)火焰产生。
【题目】食品包装中常使用一种“504双吸剂”做为保鲜剂,其成分为铁粉、生石灰等。其可用于食品保鲜的原因是可以吸收_______(写出一种物质化学式即可), 实验小组同学对一包使用过的“504双吸剂”进行了如下探究。
[提出问题]使用后固体的成分是什么?
[查阅资料]Fe+2FeCl3=3FeCl2
[进行猜想]固体成分可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3。(其它不考虑)
[进行实验]
甲同学的实验记录:
实验操作 | 实验现象 | 实验结论 |
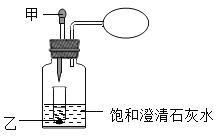
取少量固体放入试管中,滴加一定量的______,用带导管的单孔塞塞紧试管口,导管另一端伸入澄清石灰水中。 | 试管中 固体逐渐减少,有大量无色气体产生,得到浅绿色溶液,澄清石灰水变浑浊。 | 固体中一定含有____,不含Fe2O3。 |
取少量固体放入试管中,加水溶解,静置后取上层清液滴加无色酚酞溶液。 | 试管底部有不溶物,____。 | 固体中含有氧化钙和氢氧化钙。 |
[实验质疑]你认为甲同学得出的实验结论是否正确,并阐述理由:______。
乙同学的实验:
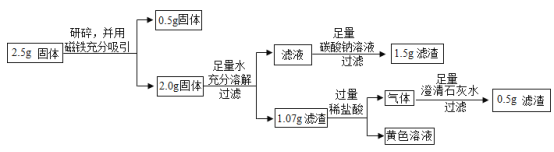
上述实验过程中加足量碳酸钠溶液时发生反应的化学方程式为_____。
[定量计算]计算乙同学实验中2.5g固体中氧化铁的质量?_____
[反思与评价]
依据甲、乙同学的实验,得出的下列结论中,正确的是_____(填字母序)。
A 甲同学实验中得到的浅绿色溶液中溶质一定有FeCl2、CaCl2
B 乙同学实验过程中共有3个反应发生
C 乙同学实验中得到的黄色溶液中溶质为FeCl3、CaCl2
D 甲、乙两位同学实验中都有气体产生,但生成的气体成分不同