题目内容
【题目】甲醛(化学式为![]() )是室内装潢时的主要污染物,下列说法不正确的是( )
)是室内装潢时的主要污染物,下列说法不正确的是( )
A.甲醛分子是由碳原子、氢分子和氧原子构成的
B.一个甲醛分子中共有6个原子
C.甲醛中碳、氢、氧三种元素的质量比为![]()
D.甲醛的相对分子质量为32
【答案】A
【解析】
A.分子由原子构成的,所以甲醛分子由碳原子、氢原子和氧原子构成,而不是由碳原子、氢分子和氧原子构成,符合题意;
B.一个甲醛分子中各原子个数之和是1+4+1=6,不符合题意;
C.物质中各元素的质量比等于各元素原子相对原子质量之和的比,所以甲醛中碳、氢、氧三种元素的质量比为12:(1×4):16=3:1:4,不符合题意;
D.相对分子质量等于各原子的相对原子质量乘以它的原子个数的代数和,所以甲醛的相对分子质量为:12+1×4+16=32,不符合题意。
故选:A。

【题目】铁的化学性质比较活泼,能与氧气、酸、CuSO4溶液等多种物质发生化学反应。化学兴趣小组在课外资料中发现,铁和Fe2O3在高温条件下竟然也能发生化学反应。
(提出问题)
铁和Fe2O3反应的产物是什么?
(查阅资料)
①FeO、Fe2O3、Fe3O4中,Fe2O3是红棕色,其余是黑色;FeO在空气中会很快被氧化成Fe2O3;Fe3O4有磁性。②二氧化碳可用作该反应的保护气。③铁的氧化物都能与酸溶液反应。
(猜想与假设)
根据质量守恒定律,请你猜想铁和Fe2O3反应的产物:
①有FeO;②只有Fe3O4;③__________。
(进行实验)
(1)按下图装好药品(铁粉过量),连好仪器(装入药品前已检查装置的气密性)。
(2)轻推注射器活塞通入二氧化碳,估计玻璃管里空气________,停止通入二氧化碳。
(3)点燃酒精喷灯加热药品,等到固体粉末全部变黑,再熄灭酒精喷灯。
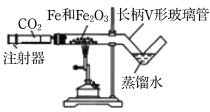
(4)当长柄V形玻璃管冷却至室温时,检验黑色粉末成分。检验过程如下(请填写表格中的空白):
检验操作及现象 | 检验结果 | |
a | 黑色粉末暴露在空气中不变化 | 黑色粉末中一定没有___________ |
b | 用磁铁靠近,黑色粉末能完全被吸引 | 黑色粉末中一定含有铁和_______ |
c | 取少量的黑色粉末装入试管,滴加足量的___________溶液,出现红色固体,充分反应后仍残留少许黑色粉末 | 确认猜想_______正确 |
(探究结论)
铁和Fe2O3能发生化合反应,有关的化学方程式是________________。
(反思评价)
本实验中的保护气,既能用二氧化碳气体,也能用________________。
【题目】某同学设计如下几组实验,探究某些酸、碱、盐之间的复分解反应能否发生。
已知:BaSO4是白色固体,难溶于水,也不与盐酸反应。
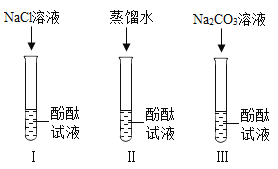
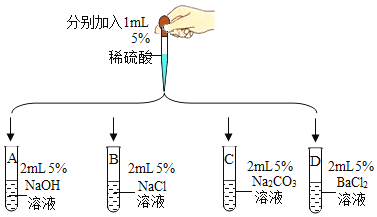
(第一组)选取5种溶液,如图所示进行实验。
实验 | 现象及结论 | 解释 |
| 试管A和B中无明显现象,不能确定反应是否发生。 | / |
(1)试管C中产生_____(填实验现象)。复分解反应已发生。 | (2)试管C中减少的微粒是_____ (填微粒符号) | |
试管D中有白色沉淀产生。复分解反应已发生。 | (3)反应的化学方程式为_____ |
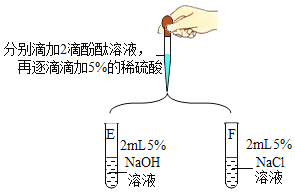
(第二组)对试管A和B中是否发生反应再探究,如图所示进行实验。
实验 | 现象及结论 | 解释 |
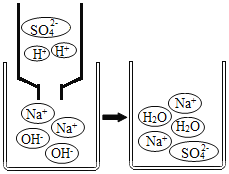
| 试管E中,滴加酚酞试液后,溶液由无色变为红色;滴加一定量稀硫酸后,溶液由红色变为无色。复分解反应已发生。 |
(4)从微观粒子变化的角度分析试管E中反应的实质是_____。 |
试管F中始终无明显现象,不能确定反应是否发生。 |
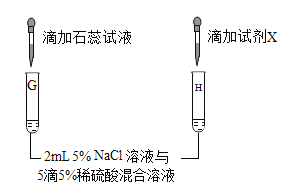
(第三组)对试管B中是否发生反应继续探究,如图所示进行实验。
实验 | 现象及结论 | 解释 |
| 试管G中溶液变红 | (5)该实验的目的是为了检验试管G的溶液中存在_____(填微粒符号)。 |
(6)向试管H中滴加_____(填“试剂X”的化学式)溶液后,有白色沉淀产生。 | 溶液中有SO42﹣存在。 | |
结论 | NaCl溶液与稀硫酸不发生复分解反应。 | |
【题目】兴趣小组在课外实验中意外发现:将镁条放入Na2CO3溶液中,快速产生较多气泡,有白色沉淀生成。小组同学对此进行了系列探究活动。
探究Ⅰ:反应产生的气体是什么?
(作出猜想)小组同学经查阅资料和讨论,根据化学变化过程中元素不变, 提出如下猜想:
①氢气;
②二氧化碳;
③氢气和二氧化碳。
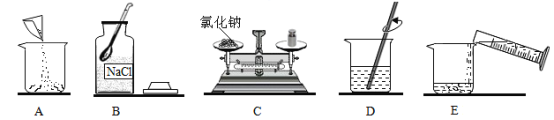
(实验1)取5g打磨后的镁条、100 mL Na2CO3溶液于装置A中,按图1所示方案进行实验。观察到的现象是_________,说明猜想①正确。
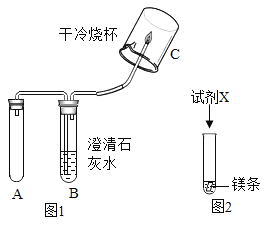
探究Ⅱ:快速产生气体的原因是什么?
(查阅资料)镁与水缓慢反应生成氢气; Na2CO3溶液显碱性,其溶液中除Na+、CO![]() 外,还有OH-。
外,还有OH-。
(作出猜想)可能是Na2CO3溶液中的某一种离子促进了镁与水的反应。
(实验2)将等质量的镁条按照图2进行如下如下实验。
实验序号 | a | b | c |
溶液(浓度相同) | H2O | Na2CO3 | NaOH |
30min时产生气体体积(mL) | <0.2 | 0.7 | <0.2 |
气体的主要成分 | H2 | ||
30min时镁条表面情况 | 大量白色固体附着 | ||
(1)实验2中a组实验的作用是_______
(2)探究2中能够说明CO![]() 对Mg与水反应起促进作用的证据是____。
对Mg与水反应起促进作用的证据是____。
探究3:反应产生的白色沉淀中是否含有MgCO3?
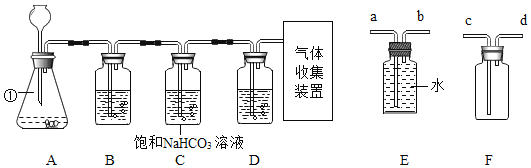
(实验3)利用如图装置证明样品中含有MgCO3(夹持仪器略去)。
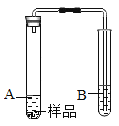
(1)所需要的试剂分别是:A___、B_____。
(2)实验中观察到的现象有___反思交流:有些伟大的发现就是从异常现象中得到启发,通过深入研究而实现的。