题目内容
【题目】下列数据是硝酸钾固体在不同温度时的溶解度.
温度/℃ | 0 | 20 | 40 | 60 | 80 |
溶解度/g | 13.3 | 31.6 | 63.9 | 110 | 169 |
(1)由上表可得到的信息是 .
(2)20℃时,向100g水中加入31.6g硝酸钾,充分溶解后得到 (填“饱和”或“不饱和”)溶液.
(3)20℃时,向100g水中加入40g硝酸钾,若使硝酸钾完全溶解,可以采用的方法是 .
(4)某标签上标有“16%的硝酸钾溶液”,由该标签可获得的信息是 、 .
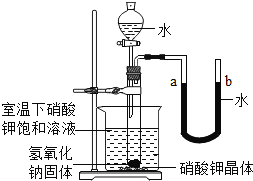
(5)右图是同学们根据所学知识设计的一个趣味实验,请参与实验并回答问题:将分液漏斗里适量的水加入大试管中,使足够量的氢氧化钠固体完全溶解后,能观察到的现象是 ;现象的主要原因是 .
【答案】(1)硝酸钾的溶解度随温度的升高而增大(其它合理答案也给分);
(2)饱和;(3)加水;
(4)该溶液中溶质是硝酸钾、溶剂是水;该溶液中溶质与溶剂的质量比是16:100;
(5)U型管中a液面下降b液面上升、烧杯中硝酸钾晶体部分溶解;氢氧化钠固体溶于水放热,试管内温度升高,气体压强增大,导致液面变化;烧杯内溶液温度升高,硝酸钾溶解度随温度升高而增大,所以部分硝酸钾晶体溶解.
【解析】(1)通过表中数据可发现,当温度不断升高时,硝酸钾的溶解度不断增大,说明硝酸钾的溶解度随温度升高而增大;从表格还可以得到几种温度下的溶解度及溶解度的大小关系等;故答案为:硝酸钾的溶解度随温度的升高而增大(其它合理答案也给分);
(2)20℃时硝酸钾的溶解度为31.6g,即此时100g水溶解31.6g硝酸钾恰好成为饱和溶液;故答案为:饱和;
(3)20℃时硝酸钾的溶解度为31.6g,即此时100g水溶解硝酸钾达饱和时只能溶解31.6g;因此,要使100g水完全溶解40g硝酸钾,可采取继续加入一定量的水的方法,故答案为:加水;
(4)16%指得是溶液中溶质的质量分数,等于溶质与溶剂的质量比,故答案为:该溶液中溶质是硝酸钾、溶剂是水;该溶液中溶质与溶剂的质量比是16:100;
(5)氢氧化钠固体溶于水放热,试管内温度升高,气体压强增大,温度的变化会引起溶解度的变化,根据曲线内容:硝酸钾溶解度随温度升高而增大,所以固体会溶解,故答案为:U型管中a液面下降b液面上升、烧杯中硝酸钾晶体部分溶解;氢氧化钠固体溶于水放热,试管内温度升高,气体压强增大,导致液面变化;烧杯内溶液温度升高,硝酸钾溶解度随温度升高而增大,所以部分硝酸钾晶体溶解.