题目内容
【题目】钙是维持人体正常功能所必需的元素,如图所示为某种补钙剂“钙尔奇”说明书的一部分,取1片钙尔奇,放入盛有10g稀盐酸的烧杯中,其中的碳酸钙跟稀盐酸恰好完全反应(其它成分与稀盐酸不反应),烧杯内物质的质量为11.34g.请你计算:

(1)每片钙尔奇中含碳酸钙的质量.
(2)使用这种补钙剂,每人每天摄入钙元素的质量.
(3)所用稀盐酸中溶质的质量分数.
【答案】每片钙尔奇中含碳酸钙的质量为1.5g,使用这种补钙剂,每人每天摄入钙元素的质量为1.2g,所用稀盐酸中溶质的质量分数为10.95%.
【解析】(1)设每片钙尔奇中CaCO3的质量为x,10g盐酸中HCl的质量为y.
完全反应后产生的二氧化碳的质量为:2g+10g﹣11.34g=0.66g
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 73 44
x y 0.66g
∴![]()
解之得:x=1.5g,y=1.095g.
(2)碳酸钙中钙元素的质量分数为:![]() ×100%=40%
×100%=40%
每天摄入的钙尔奇中钙元素的质量为:1.5g×2×40%=1.2g.
(3)所用盐酸中HCl的质量分数为:![]() ×100%=10.95%.
×100%=10.95%.
答:每片钙尔奇中含碳酸钙的质量为1.5g,使用这种补钙剂,每人每天摄入钙元素的质量为1.2g,所用稀盐酸中溶质的质量分数为10.95%.

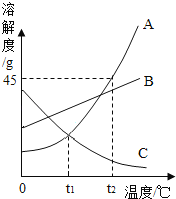
【题目】下列数据是硝酸钾固体在不同温度时的溶解度.
温度/℃ | 0 | 20 | 40 | 60 | 80 |
溶解度/g | 13.3 | 31.6 | 63.9 | 110 | 169 |
(1)由上表可得到的信息是 .
(2)20℃时,向100g水中加入31.6g硝酸钾,充分溶解后得到 (填“饱和”或“不饱和”)溶液.
(3)20℃时,向100g水中加入40g硝酸钾,若使硝酸钾完全溶解,可以采用的方法是 .
(4)某标签上标有“16%的硝酸钾溶液”,由该标签可获得的信息是 、 .
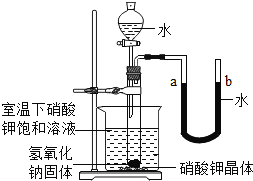
(5)右图是同学们根据所学知识设计的一个趣味实验,请参与实验并回答问题:将分液漏斗里适量的水加入大试管中,使足够量的氢氧化钠固体完全溶解后,能观察到的现象是 ;现象的主要原因是 .