题目内容
【题目】请从![]() 、
、![]() 、
、![]() 、
、![]() 四种元素中选一种或几种元素,写出符合下列要求的化学式。
四种元素中选一种或几种元素,写出符合下列要求的化学式。
(1)能供人体呼吸的气体是 ;(2)相对分子质量最小的气体是 ;
(3)天然存在最硬的物质是 ;(4)人体内含量最多的物质是 ;
【答案】(1)![]() ;(2)
;(2)![]() ;(3)
;(3)![]() ;(4)
;(4)![]() ;
;
【解析】根据组成物质的元素是氢、碳、氧、钙四种元素中选一种或几种可知,
(1)能供人体呼吸的气体是氧气,其化学式为![]() ;
;
(2)相对分子质量最小的气体是氢气,化学式为![]() ;
;
(3)天然存在最硬的物质是金刚石,其化学式为![]() ;
;
(4)人体内含量最多的物质是水,其化学式为![]() ;
;
试题分析:根据能供人体呼吸的气体是氧气,相对分子质量最小的气体是氢气,天然存在最硬的物质是金刚石,人体内含量最多的物质是水,根据化学式的书写规律,结合题目中元素种类书写化学式.

【题目】(6分)化学兴趣小组的同学对“影响金属与盐酸反应的剧烈程度的因素”进行了探究。
【提出问题】金属与盐酸反应的剧烈程度受哪些因素的影响?
【做出猜想】a.可能与金属本身的性质有关
b.可能与盐酸的浓度有关
【设计探究】实验所用的金属均已用砂纸打磨。
实验(1)为探究猜想a,小明同学分别在两支试管中放入相同质量的镁片和铁片,然后分别加入相同浓度和质量的稀盐酸,观察到放镁片的试管中立即产生大量气泡,放铁片的试管中只产生少量气泡,写出镁与盐酸反应的化学方程式 。
从实验现象可以判断:金属活动性Mg Fe(填“>”“<”或“=”)。
得出结论: 。
实验(2)为探究猜想b,小组同学设计如图装置进行实验,
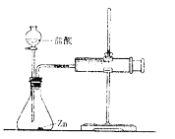
所用药品、实验数据如下表:
实验编号 | 选用金属 (均取2g) | 盐酸浓度(均取50ml) | 每30秒产生气体的体积/ml | |||||
30秒 | 30-60 秒 | 60-90秒 | 90-120秒 | 120-150秒 | 前150秒共收集气体 | |||
Ⅰ | 镁片 | 10% | 2.9 | 16.9 | 11.9 | 9.2 | 7.6 | 48.5 |
Ⅱ | 镁片 | 5% | 1.6 | 8.4 | 5.9 | 4.8 | 3.7 | 24.4 |
其中注射器的作用是 。
得出结论:金属与盐酸发生反应的剧烈程度与盐酸的浓度有关,其关系是 。
【反思评价】本题奖励4分,化学试卷总分不超过60分。
根据表中实验Ⅱ数据分析,请描述锌与盐酸发生反应快慢的变化情况并解释原因 。通过以上探究,你认为金属与盐酸反应的剧烈程度还可能受哪些因素影响,设计实验验证。 。