题目内容
【题目】如图所示实验,探究酸碱中和反应。
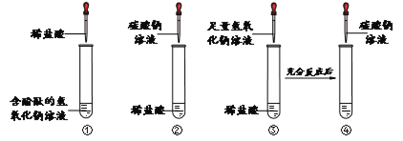
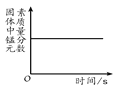
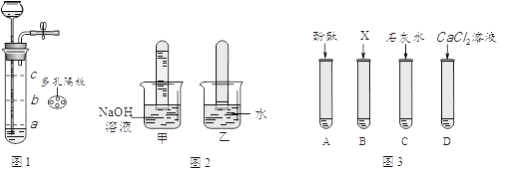
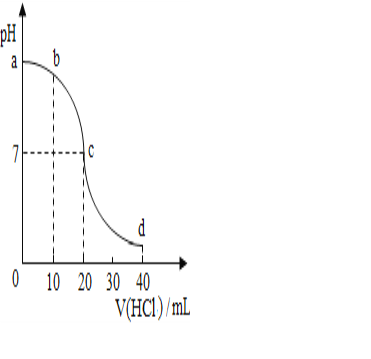
探究一:向图①中含酚酞的氢氧化钠溶液中滴加稀盐酸,边滴边振荡,并测量pH变化绘制曲线如图。
(1)图①中反应的化学方程式是___________________,该实验证明碱与酸发生反应的现象是____________________。
(2)图⑤中表示恰好完全反应的点是________(填字母),b、c、d三点处对应溶液所含溶质NaCl的质量大小关系是______________。
思路1:通过溶液酸碱性变化证明酸碱发生中和反应。
探究二:向图②稀盐酸中滴加碳酸钠溶液;向图③稀盐酸中滴加足量氢氧化钠溶液,充分反应后再滴加碳酸钠溶液如图④。
(1)图②中的现象是______________,反应的化学方程式是__________________。
(2)图④中的现象是_______________,证明酸碱发生了中和反应。
(3)设计图②实验的目的是______________。
思路2:通过________________证明酸碱发生中和反应。
【答案】 NaOH+HCl![]() NaCl+H2O 溶液从红色变为无色 c d=c>b 有气泡产生 Na2CO3 + 2HCl→2NaCl + H2O + CO2↑ 无明显现象 对比 证明反应物的消失
NaCl+H2O 溶液从红色变为无色 c d=c>b 有气泡产生 Na2CO3 + 2HCl→2NaCl + H2O + CO2↑ 无明显现象 对比 证明反应物的消失
【解析】本题主本考查酸碱中和反应,在分析时可根据PH的变化来分析,
图①是向氢氧化钠溶液中滴加稀盐酸,所以化学方程式为:
NaOH+HCl==NaCl+H2O,本来氢氧化钠中含有酚酞,酚酞显红色,滴入盐酸后碱与酸反应,当碱反应后,溶液 中不存在碱,所以红色消失。
图⑤中,当酸与碱完全反应时,溶液中不存在酸和碱,这时PH为7,所以选C,从图中分析,随着酸的滴加,生成的氯化钠渐渐增加直到反应完,所以d=c>b
图②是将碳酸钠滴入盐酸中,碳酸钠与盐酸反应生成氯化钠和水和二氧化碳,所以现象为:有气泡产生 ,化学方程式: Na2CO3 + 2HCl==2NaCl + H2O + CO2↑
(2)、图④是图3基础上滴加碳酸钠,3中加入足量的氢氧化钠,盐酸已经反应完,加入碳酸钠后不再反应,所以现象为:无明显现象
(3)图②中是向盐酸中滴加碳酸钠,有气泡生成,通过现象知道反应了,而4中同样滴加碳酸钠,但无现象,通过对比可以知道反应的情况,所以作用是:对比。酸碱发生中和反应有时无现象,不知是否发生,可以向其中滴加其他物质,让出现现象证明反应了,所以是:证明反应物的消失

 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案