题目内容
(8分)某化学兴趣小组的同学在化学氧自救器的说明书中看到“人呼出气体中的二氧化碳与自救器药罐中的生氧剂(超氧化钾KO2)接触能产生氧气”后,对自救器内发生的化学反应原理产生了探究欲望。在老师指导下,同学们展开了以下两个实验探究活动,请你参与。
(1)用下图所示的由A、B、C、D组合成的成套装置和有关药品制取并收集氧气。
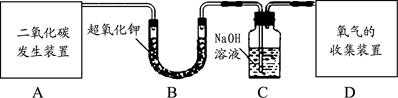
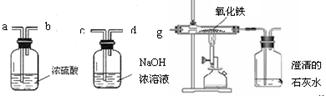
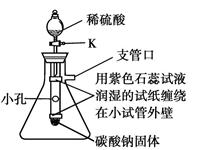
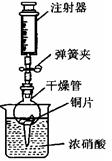
用石灰石与稀盐酸制取二氧化碳,则A中装置可采用下图中的 (填数字序号,下同);其反应方程式为 ;D中装置可采用下图中的 。

(2)二氧化碳与超氧化钾反应除生成氧气还生成什么物质?
[老师提示]1.二氧化碳与超氧化钾反应的生成物只有两种,其一是氧气,其二是一种化合物。
2. 人呼出的气体中含有的水分也能与超氧化钾反应生成氧气。
[作出猜想]二氧化碳与超氧化钾反应生成的化合物到底是哪种物质?
甲同学作出了以下三种猜想:①是一种酸; ②是一种碱; ③是一种碳酸盐。
通过对反应物有关的元素组成的分析,乙同学认为猜想 (填数字序号)一定是错误的,理由是 。
[进行实验]同学们通过以下实验验证了甲同学的另一个猜想是正确的,请完成下述实验报告.
(3)简述鉴定氧自救器药罐中生氧剂超氧化钾是否需要更换的简便的化学方法 。
(1)用下图所示的由A、B、C、D组合成的成套装置和有关药品制取并收集氧气。

用石灰石与稀盐酸制取二氧化碳,则A中装置可采用下图中的 (填数字序号,下同);其反应方程式为 ;D中装置可采用下图中的 。

(2)二氧化碳与超氧化钾反应除生成氧气还生成什么物质?
[老师提示]1.二氧化碳与超氧化钾反应的生成物只有两种,其一是氧气,其二是一种化合物。
2. 人呼出的气体中含有的水分也能与超氧化钾反应生成氧气。
[作出猜想]二氧化碳与超氧化钾反应生成的化合物到底是哪种物质?
甲同学作出了以下三种猜想:①是一种酸; ②是一种碱; ③是一种碳酸盐。
通过对反应物有关的元素组成的分析,乙同学认为猜想 (填数字序号)一定是错误的,理由是 。
[进行实验]同学们通过以下实验验证了甲同学的另一个猜想是正确的,请完成下述实验报告.
| 实验步骤 | 实验现象 | 实验结论 |
| | | |
(1)②; CaCO3 + 2HCl = CaCl2 + H2O + CO2↑ ; ③
(2)① ②
二氧化碳与超氧化钾都不含氢元素,根据质量守恒定律,不可能生成含有氢元素的酸或碱(答案合理即可)
或
(空答、错答、漏答均为0分;答案正确为2分)
(3)取待鉴定的生氧剂少量于试管中,滴加少量的水,观察是否有气泡产生,将带火星的木条伸入试管内,观察木条是否复燃,即可判断生氧剂是否需要更换。
(2)① ②
二氧化碳与超氧化钾都不含氢元素,根据质量守恒定律,不可能生成含有氢元素的酸或碱(答案合理即可)
| 实验步骤 | 实验现象 | 实验结论 |
| 将二氧化碳与超氧化钾反应后的固体取样加入稀盐酸,把产生的气体通入足量的澄清石灰水中 | 有大量气泡产生 澄清石灰水变浑浊 | 猜想 ③ (填序号)是正确的,二氧化碳与超氧化钾反应生成的化合物是 碳酸钾 |
| 实验步骤 | 实验现象 | 实验结论 |
| 将二氧化碳与超氧化钾反应后的固体取样加入蒸馏水,配成溶液,再加入澄清石灰水 | 无色溶液中出现白色浑浊 | 猜想 ③ (填序号)是正确的,二氧化碳与超氧化钾反应生成的化合物是 碳酸钾 |
(3)取待鉴定的生氧剂少量于试管中,滴加少量的水,观察是否有气泡产生,将带火星的木条伸入试管内,观察木条是否复燃,即可判断生氧剂是否需要更换。
试题分析:(1)用石灰石与稀盐酸制取二氧化碳,是固体与液体反应不要加热的类型,故A中装置可采用②;其反应方程式为CaCO3 + 2HCl = CaCl2 + H2O + CO2↑ ;因二氧化碳的密度大于空气,可溶于水,故可用向上排空气法收集,D中装置可采用③;
(2)二氧化碳与超氧化钾反应,生成物是“①是一种酸和②是一种碱”的猜想肯定是错误的,因为二氧化碳与超氧化钾都不含氢元素,根据质量守恒定律,不可能生成含有氢元素的酸或碱;
要用实验验证甲同学“③是一种碳酸盐”的猜想是正确的,可以通过如下实验来验证:
| 实验步骤 | 实验现象 | 实验结论 |
| 将二氧化碳与超氧化钾反应后的固体取样加入稀盐酸,把产生的气体通入足量的澄清石灰水中 | 有大量气泡产生 澄清石灰水变浑浊 | 猜想 ③ (填序号)是正确的,二氧化碳与超氧化钾反应生成的化合物是 碳酸钾 |
| 实验步骤 | 实验现象 | 实验结论 |
| 将二氧化碳与超氧化钾反应后的固体取样加入蒸馏水,配成溶液,再加入澄清石灰水 | 无色溶液中出现白色浑浊 | 猜想 ③ (填序号)是正确的,二氧化碳与超氧化钾反应生成的化合物是 碳酸钾 |
点评:本题的难点是设计实验来探究碳酸盐的存在,可以根据碳酸根离子的性质来设计实验,让其与稀盐酸或者澄清石灰水反应。

练习册系列答案
相关题目