题目内容
过氧化氢的水溶液俗称双氧水,在放置过程中会缓慢分解,化学方程式为:2H2O2![]() 2H2O+O2↑.现有一瓶未曾使用过的、久置的双氧水,瓶上商品标签提供了如下信息:
2H2O+O2↑.现有一瓶未曾使用过的、久置的双氧水,瓶上商品标签提供了如下信息:
①H2O2的质量分数为30%;
②内装溶液质量为1000 g;
③实验测定,其中H2O2的质量分数仅为10%.
(1)若用这瓶双氧水来配制H2O2的质量分数为3%的医用双氧水1500 g,需用这种双氧水的质量是多少?
(2)计算这瓶双氧水中已分解的过氧化氢的质量.(计算结果保留整数)
答案:
解析:
解析:
|
答:(1)需用这种双氧水的质量是450 g.(2)已分解的过氧化氢的质量为210 g 解:(1)设需要这种双氧水的质量是x,根据溶质在稀释前后质量不变,则有 10%x=1500 g×3% 解得x=450 g (2)设已分解的过氧化氢的质量为x,同时生成的氧气的质量为m. 2H2O2 68 32 x m 根据题意得: 解得x=210 g |

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
过氧化氢的水溶液俗称双氧水,在放置过程中会缓慢分解.某100g30%的双氧水放置一段时间后,经实验测定其溶质质量分数变为25%,则分解掉的过氧化氢的质量是( )
| A、5g | B、5.3g | C、5.67g | D、6.56g |
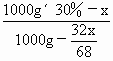 ×100%=10%
×100%=10%