题目内容
【题目】小惠在帮助学校整理实验的志愿者服务中,发现有一瓶标签破损的硫酸铜溶液,在征得老师的同意后,她对该溶液的溶质质量分数进行了下列探究活动:
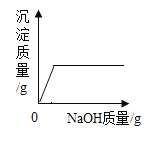
取出该溶液50g,向其中逐滴加入溶质质量分数为20%的氢氧化钠溶液,反应过程中生成沉淀的质量与所用氢氧化钠溶液质量的关系如图所示。请回答:
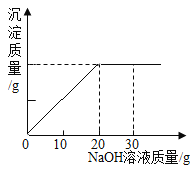
(1)硫酸铜与氢氧化钠恰好完全反应时,用去氢氧化钠溶液_____g;
(2)该硫酸铜溶液中溶质的质量分数是多少?(写出计算过程)
(3)当滴加氢氧化钠溶液质量为21g时,溶液中所含的溶质是_____。
【答案】(1)20;(2)16%(详见解析);(3)Na2SO4;NaOH
【解析】
(1)反应过程中生成沉淀的质量与所用氢氧化钠溶液质量的关系图可知,硫酸铜与氢氧化钠恰好完全反应时,用去氢氧化钠溶液20g;
(2)设硫酸铜溶液中溶质硫酸铜的质量为x
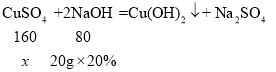
![]()
x=8g
硫酸铜溶液中溶质的质量分数=![]() × 100%=16%;
× 100%=16%;
(3)当滴加氢氧化钠溶液质量为21g时,氢氧化钠溶液过量,溶液中所含的溶质是Na2SO4 、NaOH。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目