题目内容
【题目】工业尾气硫化氢(H2S)是一种有毒气体,溶于水成为氢硫酸(H2S)溶液。目前采用氢氧化钠溶液吸收可以减少对空气的污染,并且可以制得工业产品硫化钠固体(硫化钠可溶于水)。工业流程如下图所示。
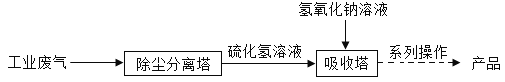
(1)可用_______________测定氢硫酸溶液的酸碱度。
(2)吸收塔内发生的是复分解反应,该反应的化学方程式为________________________________________。
(3)系列操作中一定有的步骤是____________操作。
【答案】pH试纸 ![]() 蒸发
蒸发
【解析】
(1)测定溶液的酸碱度,一般采用pH试纸,玻璃棒蘸取溶液滴加到干燥的pH试纸上,然后根据变色情况与标准比色卡对比,得出溶液的酸碱度;
故答案为:pH试纸。
(2)吸收塔内发生的是复分解反应,硫化氢与氢氧化钠反应生成硫化钠和水,据此书写化学化学方程式,书写时注意配平,所以化学方程式为![]() ;
;
故答案为:![]() 。
。
(3)硫化钠可以溶于水形成溶液,由溶液得到溶质硫化钠,就需要进出蒸发,去除溶剂;
故答案为:蒸发。

练习册系列答案
相关题目
【题目】今年“五·一”假期,小丽随爸爸到乡下省亲,期间看到许多漂亮的大理石,于是好带了一些回来,想去学校实验室测定这此大理石中CaCO3的含量。他称取了20克大理石样品置于烧杯中,然后将250g稀盐酸分成五等份,依次加入烧杯充分反应,记录有关实验数据如下表所示(大理石中其他分均不溶于水,也不参与化学反应)。
加入次数 | 一 | 二 | 三 | 四 | 五 |
加入稀盐酸的质量 | 50 | 50 | 50 | 50 | 50 |
烧杯中剩余固体的质量 | 15 | 10 | 5 | 5 | m |
试求:(1)m的值应为_____;
(2)实验中大理石样品所含CaCO3的质量分数?_____
(3)实验中所用稀盐酸的溶质质量分数?_____